题目内容
12. 乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务.该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值.通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值.
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液.
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000mol•L-1的KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL.
请回答下列问题:
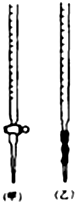
(1)滴定时,将酸性KMnO4标准液装在如图中的甲(填“甲”或“乙”)滴定管中.
(2)本实验滴定达到终点的标志是当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点.
(3)通过上述数据,求得x=2.讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会偏大(填“偏大”、“偏小”或“不变”,下同).
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会偏小.
分析 (1)高锰酸钾可氧化橡胶;
(2)高锰酸钾溶液为紫色,滴定终点时溶液显紫色;
(3)结合2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O及H2C2O4•xH2O的质量计算x;
①若滴定终点时俯视滴定管,消耗高锰酸钾溶液的体积偏小;
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,消耗高锰酸钾溶液的体积偏大,以此来解答.
解答 解:(1)KMnO4标准溶液具有强氧化性,应装在酸式滴定管中,选甲,故答案为:甲;
(2)本实验滴定达到终点的标志是:最后一滴高锰酸钾滴入后,锥形瓶内的溶液突然呈现紫色(或紫红色),且半分钟内溶液不褪色,
故答案为:当滴入最后一滴酸性KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
(3)由题给化学方程式及数据可知,1.260g纯草酸晶体中含H2C2O4的物质的量为0.1000 mol/L×10.00 mL×10-3L/mL×5/2×100 mL/25 mL=0.0100 mol,则1.260 g H2C2O4•xH2O中含H2O的物质的量为$\frac{1.260g-0.0100mol×90g/mol}{18g/mol}$=0.0200 mol,则x=2,
故答案为:2;
①若滴定终点时俯视滴定管,则所得消耗酸性KMnO4溶液的体积偏小,由此所得n(H2C2O4)偏小,则n(H2O)偏大,x偏大,故答案为:偏大;
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则消耗其体积偏大,所得x值偏小,故答案为:偏小.
点评 本题考查物质含量的测定实验,为高频考点,把握仪器的使用、氧化还原反应、实验技能为解答关键,侧重分析与实验能力的考查,注意结合反应计算,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
19.已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的有( )
①生成物的质量分数一定增加
②生成物的产量一定增大
③反应物的转化率一定增大
④正反应速率一定大于逆反应速率
⑤反应物的浓度一定降低
⑥使用了合适的催化剂.
①生成物的质量分数一定增加
②生成物的产量一定增大
③反应物的转化率一定增大
④正反应速率一定大于逆反应速率
⑤反应物的浓度一定降低
⑥使用了合适的催化剂.
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
20.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 1molN2与4molH2反应生成的NH3分子数为2NA | |
| B. | 14g乙烯和丙烯混合气体中的氢原子数为2NA | |
| C. | 1 molFe溶于过量硝酸,电子转移数为2NA | |
| D. | 标准状况下,2.24LCCl4含有的共价键数为0.4NA |
17.含有极性键且分子中各原子都满足8电子稳定结构的化合物是( )
| A. | CH4 | B. | CH2═CH2 | C. | CO2 | D. | N2 |
2.若已知标准氢氧化钠溶液的浓度为0.2000mol/L,来测定未知浓度的盐酸溶液,实验步骤如下,请完成填空
(1)仪器的洗涤:将2支滴定管和锥形瓶洗涤干净,滴定管还要润洗.
(2)在滴定管中装入相应的溶液,并记录好初读数
(3)用滴定管量取20.00ml的未知盐酸溶液于锥形瓶中,并加入2到3滴酚酞试液作为指示剂,振荡,摇匀.
(4)滴定操作:滴定时一手控制滴定管,一手摇动锥形瓶,眼睛观察锥形瓶内颜色的变化,当溶液颜色由无色变为浅红色,且半分钟内不变色时,则达滴定终点,记录读数.
(5)数据处理
该同学要做第三次实验的理由是第二次实验误差较大.
以上数据计算待测盐酸的物质的量浓度为0.1849mol/L.
(1)仪器的洗涤:将2支滴定管和锥形瓶洗涤干净,滴定管还要润洗.
(2)在滴定管中装入相应的溶液,并记录好初读数
(3)用滴定管量取20.00ml的未知盐酸溶液于锥形瓶中,并加入2到3滴酚酞试液作为指示剂,振荡,摇匀.
(4)滴定操作:滴定时一手控制滴定管,一手摇动锥形瓶,眼睛观察锥形瓶内颜色的变化,当溶液颜色由无色变为浅红色,且半分钟内不变色时,则达滴定终点,记录读数.
(5)数据处理
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.00 | 18.50 |
| 2 | 0.00 | 22.45 |
| 3 | 0.00 | 18.48 |
以上数据计算待测盐酸的物质的量浓度为0.1849mol/L.
 碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
碱式碳酸铜是一种化工原料,化学式用mCu(OH)2•nCuCO3表示.实验室以废铜屑为原料制取碱式碳酸铜的步骤如下: