题目内容
6.有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③水银 ④蔗糖 ⑤冰醋酸(纯醋酸晶体)⑥KNO3溶液 填空回答(填序号):(1)以上物质能导电的是③⑥;
(2)以上物质中属于电解质的是①②⑤;
(3)以上物质中属于弱电解质的是⑤.
分析 (1)物质有自由移动电子或离子的能导电;
(2)在水溶液中或熔融状态下能导电的化合物为电解质,包括酸、碱、盐、金属氧化物和水;
(3)在水溶液中不能完全电离的化合物为弱电解质,包括弱酸、弱碱和水.据此分析.
解答 解:①干燥的食盐晶体不能导电,且由于是混合物,故既不是电解质也不是非电解质;
②液态氯化氢不能导电,是电解质,且是强电解质;
③水银能导电,但由于是单质,故既不是电解质也不是非电解质;
④蔗糖不能导电,是非电解质;
⑤冰醋酸(纯醋酸晶体)不能导电,是电解质,且由于是弱酸,是弱电解质;
⑥KNO3溶液能导电,但由于是混合物,故既不是电解质也不是非电解质.
(1)以上物质能导电的是③⑥,故答案为:③⑥;
(2)以上物质中属于电解质的是①②⑤,故答案为:①②⑤;
(3)以上物质中属于弱电解质的是⑤,故答案为:⑤.
点评 本题考查了物质能否导电的判断以及电解质和弱电解质的判断,难度不大,应注意的是强弱电解质的本质区别是能否完全电离.

练习册系列答案
相关题目
11.用分液漏斗可将一组三种二元混合物都分开的是( )
| A. | 酒精和水.酒精和乙醚.溴苯和水 | |
| B. | 溴乙烷和水.乙酸乙酯和水.溴苯和水 | |
| C. | 溴苯和水.油脂和苯.蔗糖和葡萄糖 | |
| D. | 甘油和水.乙醛和水.乙酸和乙醇 |
12.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 盐酸与氢氧化钠反应 | D. | 氧化钙溶于水 |
1.下列说法正确的是( )
| A. | 硅、锗都位于金属与非金属的交界处,都可以做半导体材料 | |
| B. | 氢化物的沸点:H2O>NH3>HF | |
| C. | 同主族元素从上到下,单质的熔点逐渐降低 | |
| D. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 |
11.NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 32克O2所含的原子数目为NA | |
| B. | 0.5 mol H2O含有的原子数目为1.5NA | |
| C. | 1 mol H2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5 mol |
15.设NA代表阿伏伽德罗常数(NA)的值,下列说法不正确的是( )
| A. | 1molCa变成Ca2+时失去的电子数为NA | |
| B. | 同温、同压、同体积的CO和NO含有的质子数 | |
| C. | 标准状况下22.4L以任意比例混合的氢气和氧气所含分子总数均为NA | |
| D. | 常温常压下,16g氧气和臭氧(O3)的混合气体中含有NA个氧原子 |
16.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25°C,pH=2的HCl溶液中含有H+的数目为0.01NA | |
| B. | 1mol$NH_4^+$中含有10NA个质子 | |
| C. | 1mol碳烯(:CH2)中含有的电子数8NA | |
| D. | 5.6g铁粉与硝酸反应失去的电子数一定为0.3NA |

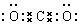 .
.