题目内容
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是 .
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是 .
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是 .
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是 .
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 ,反应所需时间的长短关系是 .
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 .
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
考点:酸碱混合时的定性判断及有关ph的计算,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)醋酸是一元弱酸、盐酸是一元强酸、硫酸是二元强酸,假设三种酸的浓度都是1mol/L时,硫酸中c(H+)为2mol/L,盐酸中c(H+)为1mol/L、醋酸中c(H+)小于1mol/L;
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力与酸最终电离出氢离子的物质的量成正比;
(3)若三者c(H+)相同时,酸的元数越大其浓度越小,酸的电离程度越大,其浓度越小;
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积与酸最终电离出氢离子的物质的量成正比;
(5)反应速率与氢离子浓度成正比,反应速率越大,反应时间越短;
(6)加水稀释促进弱电解质电离.
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力与酸最终电离出氢离子的物质的量成正比;
(3)若三者c(H+)相同时,酸的元数越大其浓度越小,酸的电离程度越大,其浓度越小;
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积与酸最终电离出氢离子的物质的量成正比;
(5)反应速率与氢离子浓度成正比,反应速率越大,反应时间越短;
(6)加水稀释促进弱电解质电离.
解答:
解:(1)醋酸是一元弱酸、盐酸是一元强酸、硫酸是二元强酸,假设三种酸的浓度都是1mol/L时,硫酸中c(H+)为2mol/L,盐酸中c(H+)为1mol/L、醋酸中c(H+)小于1mol/L,所以相同浓度时,氢离子浓度大小顺序是b>a>c,故答案为:b>a>c;
(2)酸中和NaOH的能力与酸最终电离出氢离子物质的量成正比,同体积、同物质的量浓度的三种酸,其物质的量相等,硫酸中氢离子的物质的量最大,盐酸和醋酸最终电离出氢离子的物质的量相等,所以中和NaOH的能力大小顺序为b>a=c,故答案为:b>a=c;
(3)若三者c(H+)相同时,假设都是1mol/L,硫酸浓度为0.5mol/L、盐酸浓度为1mol/L、醋酸浓度大于1mol/L,所以物质的量浓度由大到小的顺序是c>a>b(或c>a=2b),故答案为:c>a>b(或c>a=2b);
(4)酸与足量的锌反应时,相同状况下产生气体的体积与酸最终电离出氢离子的物质的量成正比,当三者c(H+)相同且体积也相同时,硫酸和稀盐酸最终电离出氢离子的物质的量相等,醋酸电离出氢离子的物质的量最大,所以这三种酸分别与足量锌反应时生成相同条件下气体体积大小顺序是c>a=b,故答案为:c>a=b;
(5)反应速率与氢离子浓度成正比,开始时氢离子浓度相等,所以其反应速率相等,即a=b=c;反应过程中,硫酸和盐酸不再电离出氢离子,醋酸继续电离生成氢离子,所以反应过程中醋酸中氢离子浓度大于硫酸、盐酸中氢离子浓度,则醋酸反应速率最大,盐酸和硫酸反应速率相等,则反应所需时间的长短关系是a=b>c,
故答案为:a=b=c;a=b>c;
(6)加水稀释时,醋酸继续电离出氢离子,硫酸和HCl不再电离出氢离子,所以稀释100倍后,c(H+)由大到小的顺序是c>a=b,故答案为:c>a=b.
(2)酸中和NaOH的能力与酸最终电离出氢离子物质的量成正比,同体积、同物质的量浓度的三种酸,其物质的量相等,硫酸中氢离子的物质的量最大,盐酸和醋酸最终电离出氢离子的物质的量相等,所以中和NaOH的能力大小顺序为b>a=c,故答案为:b>a=c;
(3)若三者c(H+)相同时,假设都是1mol/L,硫酸浓度为0.5mol/L、盐酸浓度为1mol/L、醋酸浓度大于1mol/L,所以物质的量浓度由大到小的顺序是c>a>b(或c>a=2b),故答案为:c>a>b(或c>a=2b);
(4)酸与足量的锌反应时,相同状况下产生气体的体积与酸最终电离出氢离子的物质的量成正比,当三者c(H+)相同且体积也相同时,硫酸和稀盐酸最终电离出氢离子的物质的量相等,醋酸电离出氢离子的物质的量最大,所以这三种酸分别与足量锌反应时生成相同条件下气体体积大小顺序是c>a=b,故答案为:c>a=b;
(5)反应速率与氢离子浓度成正比,开始时氢离子浓度相等,所以其反应速率相等,即a=b=c;反应过程中,硫酸和盐酸不再电离出氢离子,醋酸继续电离生成氢离子,所以反应过程中醋酸中氢离子浓度大于硫酸、盐酸中氢离子浓度,则醋酸反应速率最大,盐酸和硫酸反应速率相等,则反应所需时间的长短关系是a=b>c,
故答案为:a=b=c;a=b>c;
(6)加水稀释时,醋酸继续电离出氢离子,硫酸和HCl不再电离出氢离子,所以稀释100倍后,c(H+)由大到小的顺序是c>a=b,故答案为:c>a=b.
点评:本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,注意:同物质的量的不同酸中和碱的能力、不同酸与金属反应速率与电解质强弱无关,为易错点.

练习册系列答案
相关题目
下列实验操作中,所用仪器合理的是( )
| A、用托盘天平称取25.20gNaCl |
| B、用四氯化碳萃取碘的饱和水溶液中的碘分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出. |
| C、在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| D、用100mL容量瓶配制50mL0.1mol/L的盐酸 |
 下表是元素周期表的一部分,表中所列字母分别代表一种元素.
下表是元素周期表的一部分,表中所列字母分别代表一种元素.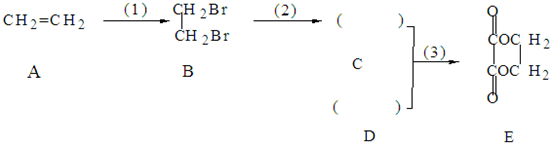
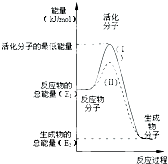 (1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.
(1)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察图,然后回答问题.