题目内容
常温下将0.010molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液,判断:
(1)溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是 和 ;
(2)溶液中n(CH3COO-)+n(OH-)-n(H+)= mol.
(1)溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是
(2)溶液中n(CH3COO-)+n(OH-)-n(H+)=
考点:酸碱混合时的定性判断及有关ph的计算,离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:将0.010molCH3COONa和0.004molHCl溶于水,由于发生CH3COO-+H+?CH3COOH,溶液中存在CH3COO-、Cl-、OH-、H+、Na+、CH3COOH和H2O等粒子,结合物料守恒和电荷守恒判断.
解答:
解:(1)根据物料守恒可知,0.010mol CH3COONa在溶液中以CH3COOH和CH3COO-存在,n(CH3COOH)+n(CH3COO-)=0.010mol,
故答案为:CH3COOH;CH3COO-;
(2)溶液遵循电荷守恒,存在:n(H+)+n(Na+)=n(Cl-)+n(CH3COO-)+n(OH-),
则n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol,
故答案为:0.006;
故答案为:CH3COOH;CH3COO-;
(2)溶液遵循电荷守恒,存在:n(H+)+n(Na+)=n(Cl-)+n(CH3COO-)+n(OH-),
则n(CH3COO-)+n(OH-)-n(H+)=n(Na+)-n(Cl-)=0.010mol-0.004mol=0.006mol,
故答案为:0.006;
点评:本题考查弱电解质的电离和盐类水解原理,物料守恒电荷守恒分析判断,掌握基础是关键,题目难度不大.

练习册系列答案
相关题目
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A、 腐蚀品 |
B、 爆炸品 |
C、 有毒气体 |
D、 易燃液体 |
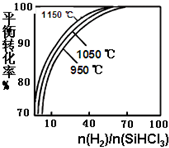 粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;
粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图; 2SO2(g)+O2(g)=2SO3(g)△H=-198kJ?mol-1反应过程的能量变化如图所示.请回答下列问题:
2SO2(g)+O2(g)=2SO3(g)△H=-198kJ?mol-1反应过程的能量变化如图所示.请回答下列问题: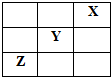 X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答:
X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答: