题目内容
7.若某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )| A. | Mg | B. | Mg | C. | $\frac{M}{6.02×1{0}^{23}}$g | D. | Mg |
分析 根据1mol任何微粒的数目均为 NA个,结合阿伏加德罗常数的含义来计算.
解答 解:根据摩尔质量可知,1mol该原子的质量是M g,1mol原子有阿伏加德罗常数NA个,即NA个原子的质量是M g,
则一个该原子的真实质量约为$\frac{M}{{N}_{A}}$=$\frac{M}{6.02×1{0}^{23}}$g,
故选C.
点评 本题考查摩尔质量、阿伏伽德罗常数等,比较基础,注意对基础知识的理解掌握,侧重于考查学生的分析能力和计算能力.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
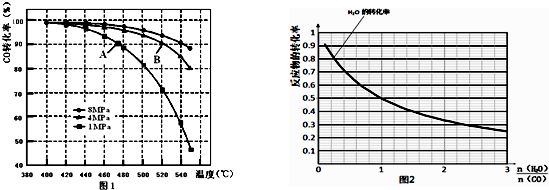
17.对于反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在其他条件不变的情况下( )
| A. | 改变压强,平衡不发生移动,反应放出的热量不变 | |
| B. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| C. | 若在原电池中进行,反应放出的热量不变 | |
| D. | 升高温度,反应速率加快,反应放出的热量不变 |
18.已知反应 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO+4H2O,当转移3mol电子时,被还原的HNO3的物质的量为( )
| A. | 4mol | B. | 2mol | C. | 1mol | D. | 3mol |
15.以X原子为中心与两个氯原子及两个碘原子相结合,形成XCl2I2分子,则以下推理中正确的是( )
| A. | 如果XCl2I2分子呈正方形结构,则没有同分异构体 | |
| B. | 如果XCl2I2分子呈正方形结构,则不可能为极性分子 | |
| C. | 如果XCl2I2分子呈四面体结构,则为极性分子 | |
| D. | 如果XCl2I2分子呈四面体结构,则有2种手性异构体 |
12.以下是25℃时几种难溶电解质的溶解度:
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子.例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可.
请回答下列问题:
(1)上述三个除杂方案都能够达到很好的效果,Fe2+、Fe3+都被转化为氢氧化铁(填名称)而除去.
(2)①中加入的试剂选择氨水为宜,其原因是不会引入新的杂质.
(3)②中除去Fe3+所发生的总反应的离子方程式为2Fe3+(aq)+3Mg(OH)2(s)═3Mg2+(aq)+2Fe(OH)3(s).
(4)下列与方案③相关的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.在pH>4的溶液中Fe3+一定不能大量存在
D.Cu2+可以大量存在于pH=4的溶液中.
| 难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可.
请回答下列问题:
(1)上述三个除杂方案都能够达到很好的效果,Fe2+、Fe3+都被转化为氢氧化铁(填名称)而除去.
(2)①中加入的试剂选择氨水为宜,其原因是不会引入新的杂质.
(3)②中除去Fe3+所发生的总反应的离子方程式为2Fe3+(aq)+3Mg(OH)2(s)═3Mg2+(aq)+2Fe(OH)3(s).
(4)下列与方案③相关的叙述中,正确的是ACD(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.在pH>4的溶液中Fe3+一定不能大量存在
D.Cu2+可以大量存在于pH=4的溶液中.
10.下列有关说法不正确的是( )
| A. | 反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H<0 | |
| B. | 为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触 | |
| C. | 常温下,将稀CH3COONa溶液加水稀释后,溶液中n(H+)•n(OH-)不变 | |
| D. | 在盛有Ca(OH)2悬浊液的绝热密闭容器中,加入少量的CaO粉末后,溶液中Ca2+数目不变,pH降低 |
 (1)同一物质存在气态的熵值最大,液态的熵值次之,固态的熵值最小.若同温同压下,一个反应生成物气体的体积等于反应物气体的体积就可粗略认为该反应的熵变为0.某化学兴趣小组,专门研究了氧族元素及其某些化学物的部分性质.所查资料如下:
(1)同一物质存在气态的熵值最大,液态的熵值次之,固态的熵值最小.若同温同压下,一个反应生成物气体的体积等于反应物气体的体积就可粗略认为该反应的熵变为0.某化学兴趣小组,专门研究了氧族元素及其某些化学物的部分性质.所查资料如下: