题目内容
18.已知反应 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO+4H2O,当转移3mol电子时,被还原的HNO3的物质的量为( )| A. | 4mol | B. | 2mol | C. | 1mol | D. | 3mol |
分析 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中Cu元素的化合价由0升高为+2价,即该反应转移3mol电子时,有1.5molCu失去电子,结合电子守恒计算.
解答 解:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O中Cu元素的化合价由0升高为+2价,即该反应转移3mol电子时,有1.5molCu失去电子,
硝酸中N元素的化合价由+5价降低为+2价,由电子守恒可知,被还原的HNO3的物质的量为$\frac{1.5mol×(2-0)}{(5-2)}$=1mol,
故选C.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化及电子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
8.下列离子方程式中,书写正确的是( )
| A. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 澄清石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 稀硫酸除铁锈:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 硫酸和Ba(OH)2反应:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
9.下列有关化学用语正确的是( )
| A. | NH4Cl的电子式: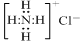 | |
| B. | 2-硝基甲苯的结构简式: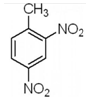 | |
| C. | 硫原子结构示意图: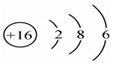 | |
| D. | 质子数为94、中子数为144的钚原子:${\;}_{94}^{144}$Pu |
6.下列叙述正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| B. | 因醋酸是弱电解质,盐酸是强电解质,因而中和等体积、等物质的量浓度的醋酸和盐酸时,盐酸消耗的NaOH比醋酸多 | |
| C. | NaHCO3溶于水,溶液中存在电离平衡 | |
| D. | 物质的量浓度相同的磷酸钠溶液和磷酸溶液中C(PO43-)相同 |
13.美国现任总统奥巴马就环境问题公开表示,到2020年,美国将会把温室气体排放量削减到1990年水平的80%,此外美国将把新能源比重提高到30%.下列说法不正确的是( )
| A. | CO2属于温室气体 | |
| B. | 太阳能电池可将太阳能转化为电能 | |
| C. | 太阳能、风能和生物能源属于新能源 | |
| D. | 乙醇属不可再生能源,乙醇燃烧不会产生温室气体 |
3.下列安全标志所表示的物质与所警示的事件不对应的是( )
| A. | 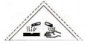 为腐蚀品,当心腐蚀 | B. |  有毒物质,当心中毒 | ||
| C. |  为易燃物质,当心火灾 | D. |  为爆炸性物质,当心爆炸 |
10.100mL6mol/L硫酸跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不能影响生成氢气的总量,可向反应物中加入适量的( )
①醋酸钠固体 ②水 ③硫酸钾固体 ④硝酸钾固体 ⑤固体铜.
①醋酸钠固体 ②水 ③硫酸钾固体 ④硝酸钾固体 ⑤固体铜.
| A. | ④⑤ | B. | ①② | C. | ①②③⑤ | D. | ①②③④ |
7.若某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )
| A. | Mg | B. | Mg | C. | $\frac{M}{6.02×1{0}^{23}}$g | D. | Mg |
1.对于常温下的下列溶液,说法正确的是( )
| A. | 常温下,向含有AgCl固体的饱和溶液,加少量水稀释,c(Ag+)和Ksp(AgCl)均保持不变 | |
| B. | pH=5的CH3COOH与CH3COONa的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 将0.2mol/LCH3COOH溶液和0.1mol/LNaOH溶液等体积混合,则反应后的混合溶液中:2c(OH-)+c(CH3COO-)=2c(H+)+c(CH3COOH) | |
| D. | 将水加热煮沸,能促进水的电离,Kw增大,pH增大,溶液呈碱性 |