题目内容
17.下列方程式书写完全正确的是( )| A. | 苯酚钠溶液中通入过量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | 溴乙烷的消去反应:C2H5Br+OH-$→_{△}^{水}$C2H4↑+Br-+H2O | |
| C. | 乙醇催化氧化成乙醛:2C2H5OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O | |
| D. | 乙酸乙酯在碱性条件下水解:CH3COOC2H5+H2O?CH3COOH+C2H5OH |
分析 A.苯酚钠溶液中通入过量二氧化碳反应生成苯酚和碳酸氢钠;
B.卤代烃消去反应条件为热的氢氧化钠的醇溶液;
C.乙醇催化氧化生成乙醛;
D.乙酸乙酯在碱性条件下完全水解生成乙酸钠和乙醇;
解答 解:A.苯酚钠溶液中通入过量二氧化碳,离子方程式:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故A错误;
B.溴乙烷与氢氧化钠的醇溶液共热发生消去反应生成乙烯和溴化钠,水,反应的化学方程式为:CH3CH2Br+NaOH$→_{醇}^{加热}$CH2=CH2↑+NaBr+H2O,故B错误;
C.乙醇催化氧化成乙醛,化学方程式:2C2H5OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,故C正确;
D.乙酸乙酯在碱性条件下水解,化学方程式:CH3COOC2H5+NaOH→CH3COONa+C2H5OH,故D错误;
故选:C.
点评 本题以有机物的结构为载体,考查有机物方程式的书写,题目难度不大,注意反应条件的标注.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
7.下列所采取的分离方法正确的是( )
| A. | 由于碘在酒精及CCl4中的溶解度大,所以可用酒精或CCl4将碘水中的碘萃取出来 | |
| B. | 水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精 | |
| C. | 苯甲酸中含有少量氯化钠,可用重结晶的方法提纯得到苯甲酸 | |
| D. | 乙酸乙酯和乙醇的混合物可以用分液的方法进行分离 |
8.下列说法正确的是( )
①苯不能使溴水因反应而褪色证明没有碳碳双键?
②苯分子中碳碳之间的键长均相等证明苯分子无单双键交替结构?
③甲苯是苯的同系物,均不能使酸性高锰酸钾溶液褪色
④间二氯苯没有同分异构体证明了苯分子不是单双键交替
⑤硝基苯中含有苯、浓硝酸、浓硫酸杂质,除杂方法是向其中加入氢氧化钠溶液后分液.
①苯不能使溴水因反应而褪色证明没有碳碳双键?
②苯分子中碳碳之间的键长均相等证明苯分子无单双键交替结构?
③甲苯是苯的同系物,均不能使酸性高锰酸钾溶液褪色
④间二氯苯没有同分异构体证明了苯分子不是单双键交替
⑤硝基苯中含有苯、浓硝酸、浓硫酸杂质,除杂方法是向其中加入氢氧化钠溶液后分液.
| A. | ①②③ | B. | ②③ | C. | ①② | D. | ④⑤ |
12.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1mol CH3+所含的电子总数为10NA | |
| C. | 0.5 mol苯分子中含有C=C双键数为1.5 NA | |
| D. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
9.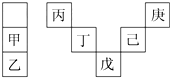 甲~庚等元素在周期表中的相对位置如表所示.己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如表所示.己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
 甲~庚等元素在周期表中的相对位置如表所示.己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如表所示.己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁的最高价氧化物是人类将太阳能转换为电能的常用材料 |
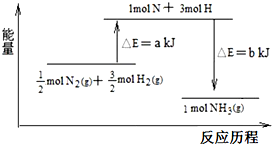
 ,则A的结构简式为
,则A的结构简式为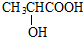 .
.