题目内容
20.有关键能数据如表:| 化学键 | Si-O | O=O | Si-Si |
| 键能kJ•mol-1 | 460 | 498.8 | X |
| A. | 423.3 | B. | 352 | C. | 920 | D. | 176 |
分析 反应中焓变等于反应物中键能之和减去生成物键能之和,以此来解答.
解答 解:Si(s)+O2(g)═SiO2(s)△H=-989.2kJ•mol-1,
焓变等于反应物中键能之和减去生成物键能之和,则
X×2+498.8-4×460=-989.2,
解得X=176,
故选D.
点评 本题考查反应热与焓变,为高频考点,把握焓变与物质中键能的关系为解答的关键,侧重分析与计算能力的考查,注意物质中化学键判断为解答的难点,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
10.下列关于平衡常数说法正确的是( )
| A. | 增大反应物的浓度,平衡常数K增大 | B. | 加大体系压强,平衡常数K增大 | ||
| C. | 加入负催化剂,平衡常数K减小 | D. | 升高温度,平衡常数K发生变化 |
11.下列说法正确的是( )
| A. | 化学反应都伴随着热量的变化 | |
| B. | 个别化学反应与能量变化无关 | |
| C. | 某些吸热反应在不加热条件下也能发生 | |
| D. | 放热反应的发生无需任何条件 |
8.已知:4HCl(g)+O2 (g)?12C12 (g)+2H2O(g)△H=-123kJ.mol-1.其中相关的化学键键能数据如下:
其中a值为( )
| 化学键 | H-Cl | O═O | Cl-Cl | H-O |
| E/(kJ•mol-1) | 431 | 397 | a | 465 |
| A. | 242 | B. | 303.5 | C. | 180.5 | D. | 365 |
15.根据如图所示情况,判断下列说法中正确的是 ( )
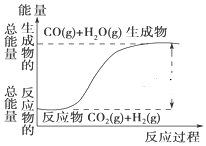

| A. | 其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=41kJ•mol-1 | |
| B. | 该反应为吸热反应 | |
| C. | 该反应为放热反应 | |
| D. | 当H2O为液态时,其反应热值大于41kJ•mol-1. |
5.肼(H2N-NH2)是一种高能燃料,有关化学反应的为N2H4(g)+O2═N2(g)+2H2O(g)△H=-576KJ/mol,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,H-O为463则断裂1molN-H键所需的能量(kJ)是( )
| A. | 391 | B. | 194 | C. | 516 | D. | 658 |
12.合成氨及其相关工业中,部分物质间的转化关系如图:下列说法不正确的是( )
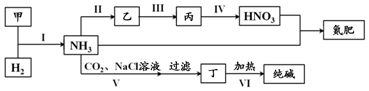

| A. | 甲、乙、丙三种物质中都含有氮元素 | |
| B. | 反应II、III和Ⅳ的氧化剂相同 | |
| C. | VI的产物可在上述流程中被再次利用 | |
| D. | V中发生反应:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl |
9.下列图示实验正确的是( )
| A. | 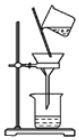 除去粗盐溶液中不溶物 | B. |  碳酸氢钠受热分解 | ||
| C. | 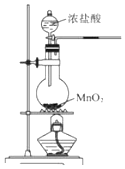 制取少量Cl2 | D. | 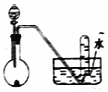 稀硝酸与铜的反应制取并收集NO |