题目内容
小王同学准备用CuSO4?5H2O配制480mL 1mol/L的溶液.
(1)小王同学选用的容量瓶容积的规格是 mL;
(2)配制好的溶液呈 色.小王同学还想通过实验证实溶质中含有SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应离子方程式.
(3)物质的量浓度误差分析:
(填偏高、偏低或无影响)
①若容量瓶洗净后未干燥,残留少量水,则所配制的溶液浓度将 ;
②定容时,若眼睛俯视,则所配制的溶液浓度将 .
(1)小王同学选用的容量瓶容积的规格是
(2)配制好的溶液呈
| 溶质 | 加入试剂 | 离子方程式 |
| SO42- |
(填偏高、偏低或无影响)
①若容量瓶洗净后未干燥,残留少量水,则所配制的溶液浓度将
②定容时,若眼睛俯视,则所配制的溶液浓度将
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)依据实验室常用容量瓶的规格选择;
(2)铜离子呈蓝色;硫酸根离子的检验:向溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生;
(3)物质的量浓度误差分析可以依据浓度公式C=
,凡是使加入的溶质的物质的量偏大或者使溶液的体积偏小的操作,都会使所配溶液的浓度偏大,凡是使加入的溶质的物质的量偏小或者使溶液的体积偏大的操作,都会使所配溶液的浓度偏大,据此分析.
(2)铜离子呈蓝色;硫酸根离子的检验:向溶液中加入盐酸使之酸化,再加入BaCl2溶液,有白色沉淀产生;
(3)物质的量浓度误差分析可以依据浓度公式C=
| n |
| V |
解答:
解:(1)配制500mL 1mol/L的溶液应选择500ml规格容量瓶,故答案为:500;
(2)硫酸铜溶液呈蓝色;取少量溶液于试管中,加几滴稀盐酸酸化,再加入几滴氯化钡溶液,若有白色沉淀,则说明含有硫酸根离子,离子方程式:Ba2++SO42-=BaSO4,故答案为:蓝;BaCl2 溶液;Ba2++SO42-=BaSO4;
(3)①溶液配制过程需加水定容,容量瓶使用时未干燥,对所配溶液浓度无影响,故答案为:无影响;
②定容时,若眼睛俯视,会导致定容时加入的蒸馏水偏少,所配溶液的体积偏小,依据浓度公式C=
可知,配得的溶液浓度偏高,故答案为:偏高.
(2)硫酸铜溶液呈蓝色;取少量溶液于试管中,加几滴稀盐酸酸化,再加入几滴氯化钡溶液,若有白色沉淀,则说明含有硫酸根离子,离子方程式:Ba2++SO42-=BaSO4,故答案为:蓝;BaCl2 溶液;Ba2++SO42-=BaSO4;
(3)①溶液配制过程需加水定容,容量瓶使用时未干燥,对所配溶液浓度无影响,故答案为:无影响;
②定容时,若眼睛俯视,会导致定容时加入的蒸馏水偏少,所配溶液的体积偏小,依据浓度公式C=
| n |
| V |
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如下图所示.Z元素原子核外K层与M层电子数相等.下列说法中正确的( )
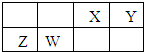

| A、Y元素最高价氧化物对应的水化物化学式为H3YO4 |
| B、原子半径由小到大的顺序为:X<Z<Y<W |
| C、与同浓度的盐酸反应,Z比W更剧烈 |
| D、W的金属性比Z的强 |
下列有关物质的性质的说法正确的是( )
| A、金刚石、C60都有较大的硬度和较高的熔点 |
| B、在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C、Cl2、SO2都可以使品红溶液褪色 |
| D、镁、铁等金属在一定条件下与水反应都生成对应的氢氧化物和氢气 |
98%的浓硫酸(密度为1.84g?cm-3)配制0.5mol?L-1的稀硫酸180mL,现给出下列仪器(配制过程中可能用到):①50mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤250mL容量瓶;⑥胶头滴管;⑦玻璃棒.配置过程一定需要使用的仪器是( )
| A、②③⑤⑥⑦ |
| B、③④⑤⑥⑦ |
| C、①②③⑤⑥⑦ |
| D、①③⑤⑥ |
已知甲为恒温、乙为恒压容器.两容器中均充入1molN2、3molH2,初始时两容器的温度、体积相同.一段时间后反应达到平衡,为使两容积中的N2在平衡混合物中的物质的量分数相同,下列措施中不可行的是( )
| A、向甲容器中充入一定量的氦气 |
| B、向乙容器中充入一定量的N2 |
| C、升高乙容器的温度 |
| D、增大甲容器的压强 |
在下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计的水银球在蒸馏烧瓶的支管口处 |
| C、过滤时,玻璃棒在引流过程中应放在三层滤纸处 |
| D、称量时,称量物放在称量纸上,置于托盘天平左盘,砝码直接放在托盘天平右盘 |