题目内容
4.已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
(1)A分子中官能团的名称是碳碳双键,D中官能团的名称是羧基,反应①的反应类型是加成反应.
(2)反应②的化学方程式是2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
反应④的化学方程式是CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O.
(3)E是常见的高分子材料,合成E的化学方程式是nCH2=CH2$\stackrel{催化剂}{→}$
 .
.(4)某同学用如图2所示的实验装置制取少量乙酸乙酯.
实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的原因是防止倒吸.
②上述实验中饱和碳酸钠溶液的作用是BC(填字母).
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
③在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,不能(能/不能)生成1mol 乙酸乙酯,原因是该反应为可逆反应,有一定的限度,不可能完全转化.
分析 有机物A的产量可以用来衡量一个国家的石油化工发展水平,则A是CH2=CH2,CH2=CH2和H2O反应生成B是CH3CH2OH,CH3CH2OH被O2氧化生成C,C进一步氧化生成D,则C是CH3CHO,D是CH3COOH,乙酸与乙醇发生酯化反应生成CH3COOCH2CH3,E是常见的高分子材料,则乙烯发生加聚反应生成E结构简式为 .
.
解答 解:有机物A的产量可以用来衡量一个国家的石油化工发展水平,则A是CH2=CH2,CH2=CH2和H2O反应生成B是CH3CH2OH,CH3CH2OH被O2氧化生成C,C进一步氧化生成D,则C是CH3CHO,D是CH3COOH,乙酸与乙醇发生酯化反应生成CH3COOCH2CH3,E是常见的高分子材料,则乙烯发生加聚反应生成E结构简式为 .
.
(1)A是CH2=CH2,含有的官能团为碳碳双键,D是CH3COOH,含有的官能团是羧基,反应①的反应类型是加成,
故答案为:碳碳双键;羧基;加成.
(2)反应②为乙醇的催化氧化反应,反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
反应④是乙酸和乙醇的酯化反应,反应化学方程式是:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O;
(3)E是聚乙烯,乙烯发生加聚反应生成聚乙烯,反应方程式为:nCH2=CH2$\stackrel{催化剂}{→}$ ,
,
故答案为:nCH2=CH2$\stackrel{催化剂}{→}$ ;
;
(4)①实验开始时,试管甲中的导管不伸入液面下是为了防止倒吸,故答案为:防止倒吸;
②饱和Na2CO3溶液能溶解乙醇,能和乙酸反应生成二氧化碳和可溶性的乙酸钠,能降低乙酸乙酯溶解度,从而更好的析出乙酸乙酯,
故答案为:BC;
③在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,不能生成1mol乙酸乙酯,因为该反应是可逆反应,当反应达到一定限度时达到平衡状态,
故答案为:不能;该反应为可逆反应,有一定的限度,不可能完全转化.
点评 本题考查有机物推断和乙酸乙酯的制取,涉及烯烃、醇、醛、羧酸的性质与转化,比较基础,注意乙酸乙酯制取中饱和碳酸钠溶液的作用.

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案| A. | 过滤 | B. | 蒸馏 | C. | 蒸发 | D. | 萃取 |
| A. | 苯、四氯化碳、无水乙醇、己烯 溴水 | |
| B. | MnO2、FeS、CuO、CuS 稀硫酸 | |
| C. | 甲酸、乙酸、乙醛、乙醇 新制氢氧化铜悬浊液 | |
| D. | 苯酚溶液、甲苯、乙酸乙酯、乙酸 饱和碳酸钠溶液 |
(1)向100mL上述溶液中加入足量BaCl2溶液,反应后将浊液过滤、洗涤、干燥,得沉淀2.33g,向沉淀中加入过量的盐酸,过滤、洗涤、干燥,得沉淀2.33g.
(2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体560mL(已换算成标准状况,假定产生的气体全部逸出).
由此可以得出关于原溶液组成的正确结论是( )
| A. | 一定存在SO42-、NH4+、Cl-,一定不存在CO32- | |
| B. | c(SO42-)=0.1mol•L-1,c(Cl-)>c(SO42-) | |
| C. | 一定存在SO42-、CO32-、NH4+,可能存在Na+ | |
| D. | 一定存在SO42-、NH4+,可能存在Na+、Cl- |
| A. | Uuo的原子序数为118 | B. | ${\;}_{118}^{297}Uuo$的核内中子数为179 | ||
| C. | ${\;}_{118}^{297}Uuo$的核外电子数为118 | D. | Uuo的相对原子质量为297 |
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | NH4NO3晶体中含共价键,是共价化合物 | |
| C. | H2O2、N2H4分子中只含有极性共价键 | |
| D. | 某化合物熔融状态能导电,可以证明该化合物内一定存在离子键 |



 CH3COOCH2CH3+H2O;反应类型:酯化反应.
CH3COOCH2CH3+H2O;反应类型:酯化反应. ;反应类型:加聚反应.
;反应类型:加聚反应.

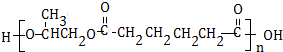 .
. .
.