题目内容
1.配制一定物质的量浓度的NaOH溶液时,能造成所配溶液浓度偏低的原因是( )| A. | 定容时俯视液面 | B. | 未洗涤烧杯和玻璃棒 | ||
| C. | 容量瓶未干燥 | D. | 转移溶液前溶液未冷却至室温 |
分析 分析操作对溶质的物质的量n和溶液体积V的影响,依据C=$\frac{n}{V}$进行误差分析,反应使n偏小或使V偏大的操作,溶液浓度都偏低,凡是使n偏达或使V偏小的操作,溶液浓度都偏高,据此分析解答.
解答 解:A.定容时俯视液面,导致溶液体积偏小,依据C=$\frac{n}{V}$可知溶液浓度偏高,故A不选;
B.未洗涤烧杯和玻璃棒,导致部分溶质损耗,溶质的物质的量偏小,依据C=$\frac{n}{V}$可知溶液浓度偏低,故B选;
C.容量瓶未干燥,对溶质的物质的量n和溶液体积V都不产生影响,溶液浓度不受影响,故C不选;
D.转移溶液前溶液未冷却至室温,冷却后,液面下降,溶液体积偏小,依据C=$\frac{n}{V}$可知溶液浓度偏高,故D不选;
故选:B.
点评 本题考查了一定物质的量浓度溶液配制误差分析,明确配制原理,准确把握操作对溶质的物质的量n和溶液体积V的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
12.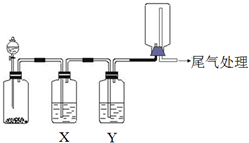 利用如图装置可以进行实验并能达到实验目的是( )
利用如图装置可以进行实验并能达到实验目的是( )
 利用如图装置可以进行实验并能达到实验目的是( )
利用如图装置可以进行实验并能达到实验目的是( )| 选项 | 实验目的 | X中试剂 | Y中试剂 |
| A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
| B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
| C | 验证电石与饱和食盐水反应生成的气体的性质并收集 | CuSO4溶液 | KMnO4 溶液 |
| D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关物质的同分异构体(不考虑立体异构)数目分、的分析中正确的是( )
| 选项 | A | B | C | D |
| 分子式 | C3H8O | C3H8 | C7H16 | C8H10 |
| 限定条件 | 能与钠反应 | 二氯化物 | 分子中还有3哥甲基 | 芳香烃、能得到3中硝基化物 |
| 同分异构体数目 | 2 | 3 | 2 | 3 |
| A. | A | B. | B | C. | C | D. | D |
16.将下列各组物质按酸、碱、盐分类顺序排列,其中正确的是( )
| A. | 硫酸、纯碱、漂白粉 | B. | 硫酸、烧碱、小苏打 | ||
| C. | 硫酸氢钠、生石灰、醋酸钠 | D. | 磷酸、熟石灰、苛性钠 |
13. T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
(1)TY2是一种常用的溶剂,是非极性分子(填“极性分子”或“非极性分子”),分子中存在2个σ 键.W的最简单氢化物容易液化,理由是分子间存在氢键.
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$cm(用含立方根的式子表示);ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2═ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂
B.HO2是氧化产物
C.HO2在碱中能稳定存在
D.1molZ参加反应有1mol电子发生转移.
 T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ•mol,I2=1817kJ•mol-1,I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$cm(用含立方根的式子表示);ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2═ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂
B.HO2是氧化产物
C.HO2在碱中能稳定存在
D.1molZ参加反应有1mol电子发生转移.
10.下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
| A. | NaClO 溶液中通入过量SO2 ClO -+SO2+H2O═HClO+HSO3- | |
| B. | 甲醇、氧气和氢氧化钾溶液组成的燃料电池的负极反应CH3OH+H2O-6e-═CO2↑+6H+ | |
| C. | AlCl3 溶液中投入过量Na:Al3++4Na+2H2O═AlO2 -+4Na++2H2↑ | |
| D. | 向明矾溶液中滴加Ba(OH)2,恰好使SO42- 沉淀完全:2Al3++3SO4 2-+3Ba2++6OH -═2Al(OH)3↓+3BaSO4↓ |