题目内容
下列说法中,正确的是( )
| A、反应产物的总能量大于反应物的总能量时,△H<0 |
| B、在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
| C、△H<0、△S>0的反应在温度低时不能自发进行 |
| D、一个化学反应的△H仅与反应的起始状态和反应的最终状态有关,与反应途径无关 |
考点:焓变和熵变
专题:
分析:A、反应热等于生成物能量和与反应物能量和的差;
B、催化剂只改变反应速率,不改变化学反应进行的方向;
C、根据△G=△H-T?△S判断;
D、△H=生成物的能量和-反应物的能量和.
B、催化剂只改变反应速率,不改变化学反应进行的方向;
C、根据△G=△H-T?△S判断;
D、△H=生成物的能量和-反应物的能量和.
解答:
解:A、△H=生成物能量和-反应物能量和,当生成物能量和大于反应物时,△H>0,故A错误;
B、催化剂只改变反应速率,不改变化学反应进行的方向,故B错误;
C、根据△G=△H-T?△S判断,对于△H<0、△S>0的反应在温度低时,如△G<0,反应能自发进行,故C错误;
D、△H=生成物的能量和-反应物的能量和,所以反应热只与反应体系的始态和终点状态有关,而与反应的途径无关,故D正确;
故选D.
B、催化剂只改变反应速率,不改变化学反应进行的方向,故B错误;
C、根据△G=△H-T?△S判断,对于△H<0、△S>0的反应在温度低时,如△G<0,反应能自发进行,故C错误;
D、△H=生成物的能量和-反应物的能量和,所以反应热只与反应体系的始态和终点状态有关,而与反应的途径无关,故D正确;
故选D.
点评:本题考查反应热与焓变,题目难度中等,注意反应能否自发进行的判断方法,学习中深刻理解相关概念,为易错点.

练习册系列答案
相关题目
有BaCl2和KCl的混合溶液100mL,将它分成两等份.一份滴加0.1mol?L-1稀硫酸25mL,使Ba2+完全沉淀;另一份滴加0.2mol?L-1 AgNO3溶液75mL,使Cl-完全沉淀.据此得知原混合溶液中的K+的物质的量浓度为( )
| A、0.1 mol?L-1 |
| B、0.125mol?L-1 |
| C、0.2 mol?L-1. |
| D、0.25mol?L-1 |
光导纤维的主要成分是( )
| A、硅 | B、玻璃 | C、二氧化硅 | D、沙子 |
下列反应中属于氧化还原反应,且水既不作氧化剂又不作还原剂的是( )
| A、SO3+H2O=H2SO4 | ||||
| B、Cl2+H2O=HCl+HClO | ||||
| C、2F2+2H2O=4HF+O2 | ||||
D、C+H2O
|
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )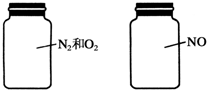

| A、所含质子数相等 |
| B、气体密度相等 |
| C、所含原子数相等 |
| D、摩尔质量相等 |
在一定温度下,容积不变的密闭容器中发生反应:C(s)+H2O(g)?CO(g)+H2(g),下列叙述不能认定该可逆反应已经达到平衡状态的是( )
| A、混合气体压强不再发生变化 |
| B、混合气体质量不再发生变化 |
| C、反应中CO与H2的物质的量之比为1:1 |
| D、生成nmolCO的同时生成nmolH2O |
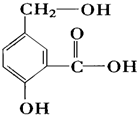 (1)用工业酒精制造的假酒中通常含有
(1)用工业酒精制造的假酒中通常含有