题目内容
9.CaCO3和盐酸反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示:
请用离子方程式表示B-C段发生的反应:Ca2++CO32-=CaCO3↓.
分析 上述反应至无气泡逸出后,取适量残留溶液,含氯化钙,逐滴滴入碳酸钠溶液,由B-C段pH=7,可知反应生成碳酸钙沉淀和NaCl,以此来解答.
解答 解:由图可知,上述反应至无气泡逸出后,取适量残留溶液,含氯化钙,逐滴滴入碳酸钠溶液,由B-C段pH=7,可知反应生成碳酸钙沉淀和NaCl,离子反应为Ca2++CO32-=CaCO3↓,故答案为:Ca2++CO32-=CaCO3↓.
点评 本题考查离子反应方程式的书写,为高频考点,把握图象及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列反应中不属于氧化还原反应的是( )
| A. | 一氧化碳通过灼热的氧化铁 | B. | 氧化铝溶于盐酸 | ||
| C. | 过氧化钠固体中通人水蒸气 | D. | 氢氧化亚铁露置在空气中 |
4.单晶硅是制作电子集成电路的基础材料.科学家预计,到2011年一个电脑芯片上将会集成10亿个晶体管,其功能远比我们想象的要大的多,这对硅的纯度要求很高.用化学方法可制得高纯度硅,其化学方程式为:
①SiO2+2C$\frac{\underline{\;高温\;}}{\;}$ Si+2CO
②Si+2Cl2$\frac{\underline{\;点燃\;}}{\;}$SiCl4
③SiCl4+2H2Si+4HCl,
其中,反应②属于( )
①SiO2+2C$\frac{\underline{\;高温\;}}{\;}$ Si+2CO
②Si+2Cl2$\frac{\underline{\;点燃\;}}{\;}$SiCl4
③SiCl4+2H2Si+4HCl,
其中,反应②属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
14.取一定量的Fe、Cu的混合物粉末,平均分成A、B、C、D、E五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(惟一还原产物)的体积及所得剩余物的质量记录如表(所有体积均在标准状况下测定):
(1)A组实验后17.2g剩余固体为Fe、Cu,B组实验后8g剩余固体为Cu.(均填写化学式)
(2)实验中每次所取混合物中铁的物质的量为0.20mol.
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:Fe2+、Cu2+、Fe3+,物质的量之比是:n(Fe2+):n(Cu2+):n(Fe3+)=6:9:2.
| 实验序号 | A | B | C | D | E |
| 硝酸溶液体积 | 100ml | 200mL | 300mL | 400mL | 500mL |
| 剩余固体的质量 | 17.2g | 8g | 0g | 0g | 0g |
| 气体体积 | 2.24L | 4.48L | 6.72L | 7.84L | 7.84L |
(2)实验中每次所取混合物中铁的物质的量为0.20mol.
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:Fe2+、Cu2+、Fe3+,物质的量之比是:n(Fe2+):n(Cu2+):n(Fe3+)=6:9:2.
19.除去括号内杂质的试剂或方法错误的是( )
| A. | KNO3晶体(NaCl),蒸馏水,结晶 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| D. | C2H5OH(CH3COOH),加足量CaO,蒸馏 |
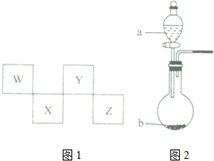 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.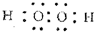 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族.