题目内容
20.共价键、离子键和分子间作用力是微粒之间的不同作用力,下列①Na2O2 ②He③NaOH④金刚石 ⑤NaCl ⑥干冰,含有其中两种结合力的是( )| A. | ①②⑤ | B. | ①③⑥ | C. | ②④⑥ | D. | ①②③⑥ |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,分子晶体中分子之间存在范德华力,据此分析解答.
解答 解:①Na2O2中钠离子和过氧根离子之间存在离子键、O原子和O原子之间存在共价键,所以过氧化钠中存在两种结合力,故正确;
②氦气只存在范德华力,故错误;
③NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在共价键,所以过氧化钠中存在两种结合力,故正确;
④金刚石中C原子之间只存在共价键,所以只存在一种结合力,故错误;
⑤NaCl中钠离子和氯离子之间存在离子键,所以只存在一种结合力,故错误;
⑥干冰中C与O原子之间存在共价键、分子之间存在范德华力,所以存在两种结合力,故正确;
故选B.
点评 本题考查了物质中存在的结合力,明确物质的构成微粒及微粒间的作用力是解本题关键,题目难度不大,注意He晶体只有分子间作用力,不含有共价键.

练习册系列答案
相关题目
11.下列有关能量转换的说法正确的是 ( )
| A. | 煤燃烧是热能转化为化学能的过程 | |
| B. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| C. | 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 | |
| D. | 化石燃料属于一次能源,电能属于二次能源 |
8.下列物质属于同系物的是( )
| A. | CH3CH2Cl与CH3CH2CH2Br | B. | 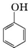 与 与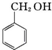 | ||
| C. | 乙酸与HCOOCH3 | D. | CH3CH2CH2OH与CH3OH |
15.你认为下列说法不正确的是( )
| A. | 氢键存在于分子之间,不存在于分子之内 | |
| B. | 对于组成和结构相似的分子,其范德华力随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
5.下列表中括号内的物质为所含的少量杂质,请选用最佳的试剂和操作方法将杂质除去,将对应的编号填入表中.试剂:a生石灰,b 溴水,c饱和碳酸钠溶液,d 酸性高锰酸钾溶液,e水.操作方法:A分液,B洗气,C蒸馏,D结晶.
| 需加入的试剂 | 操作方法 | |
| CH3CH2OH(水) | 蒸馏 | |
| 乙烷(乙烯) | 洗气 | |
| 乙酸乙酯(乙酸,乙醇) |
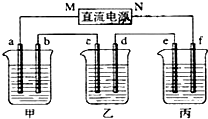
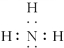
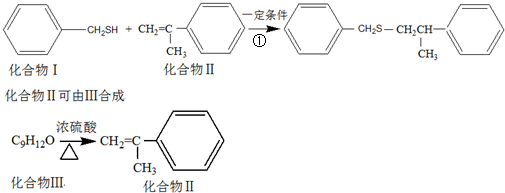
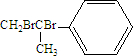 .
.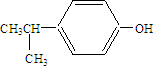 .
.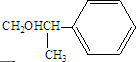 .化合物Ⅳ与新制Cu(OH)2反应的化学方程式
.化合物Ⅳ与新制Cu(OH)2反应的化学方程式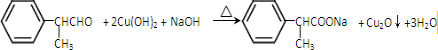 .
.