题目内容
部分弱酸的电离平衡常数如下表:
下列选项正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) |
Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A、2CN-+H2O+CO2═2HCN+CO32- |
| B、中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
| C、物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-) |
| D、c(NH4+)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,c(NH4HCO3)>c(NH4CN)>c(HCOONH4) |
考点:离子浓度大小的比较,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A.酸的电离平衡常数越大,酸的酸性越强,根据强酸制取弱酸解答;
B.等pH的HCOOH和HCN,酸的电离平衡常数越大,该酸的浓度越小,等体积等pH的不同酸消耗NaOH的物质的量与酸的物质的量成正比;
C.酸的电离平衡常数越大,则其酸根离子水解程度越小,酸的电离平衡常数HCOOH>HCN,则酸根离子水解程度HCOO-<CN-,所以溶液中阴离子浓度c(HCOO-)>c(CN-);
D.酸的电离平衡常数越大,其酸根离子水解程度越小,促进铵根离子水解程度越小,则相同浓度的这几种盐溶液中铵根离子浓度越大.
B.等pH的HCOOH和HCN,酸的电离平衡常数越大,该酸的浓度越小,等体积等pH的不同酸消耗NaOH的物质的量与酸的物质的量成正比;
C.酸的电离平衡常数越大,则其酸根离子水解程度越小,酸的电离平衡常数HCOOH>HCN,则酸根离子水解程度HCOO-<CN-,所以溶液中阴离子浓度c(HCOO-)>c(CN-);
D.酸的电离平衡常数越大,其酸根离子水解程度越小,促进铵根离子水解程度越小,则相同浓度的这几种盐溶液中铵根离子浓度越大.
解答:
解:酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,则酸根离子水解程度CO32->CN->HCO3->HCOO-,
A.酸的电离平衡常数越大,酸的酸性越强,强酸能够制取弱酸,所以二者反应生成HCN和HCO3-,离子方程式为CN-+H2O+CO2═HCN+HCO3-,故A错误;
B.等pH的HCOOH和HCN,c(HCN)>c(HCOOH),等体积、等pH的HCOOH和HCN,n(HCN)>n(HCOOH),中和等pH等体积的HCOOH和HCN,消耗NaOH的量前者小于后者,故B正确;
C.酸的电离平衡常数HCOOH>HCN,则酸根离子水解程度HCOO-<CN-,所以溶液中阴离子浓度c(HCOO-)>c(CN-),物质的量浓度相等的HCOONa和KCN,则c(Na+)=c(K+),所以c(Na+)-c(HCOO-)<c(K+)-c(CN-),故C正确;
D.酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,则酸根离子水解程度CO32->CN->HCO3->HCOO-,促进铵根离子水解程度大小顺序是CO32->CN->HCO3->HCOO-,则相同浓度的这几种盐溶液中c(NH4+)大小顺序是c(NH4CN)<c(NH4HCO3)<c(HCOONH4),所以c(NH4+)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中c(NH4CN)>c(NH4HCO3)>c(HCOONH4),故D错误;
故选BC.
A.酸的电离平衡常数越大,酸的酸性越强,强酸能够制取弱酸,所以二者反应生成HCN和HCO3-,离子方程式为CN-+H2O+CO2═HCN+HCO3-,故A错误;
B.等pH的HCOOH和HCN,c(HCN)>c(HCOOH),等体积、等pH的HCOOH和HCN,n(HCN)>n(HCOOH),中和等pH等体积的HCOOH和HCN,消耗NaOH的量前者小于后者,故B正确;
C.酸的电离平衡常数HCOOH>HCN,则酸根离子水解程度HCOO-<CN-,所以溶液中阴离子浓度c(HCOO-)>c(CN-),物质的量浓度相等的HCOONa和KCN,则c(Na+)=c(K+),所以c(Na+)-c(HCOO-)<c(K+)-c(CN-),故C正确;
D.酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,则酸根离子水解程度CO32->CN->HCO3->HCOO-,促进铵根离子水解程度大小顺序是CO32->CN->HCO3->HCOO-,则相同浓度的这几种盐溶液中c(NH4+)大小顺序是c(NH4CN)<c(NH4HCO3)<c(HCOONH4),所以c(NH4+)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中c(NH4CN)>c(NH4HCO3)>c(HCOONH4),故D错误;
故选BC.
点评:本题考查了离子浓度大小比较,明确酸的电离平衡常数与酸的强弱、酸根离子水解程度大小之间的关系是解本题关键,再结合物料守恒、物质的性质等知识点来分析解答,易错选项是D,会采用逆向思维的方法确定盐溶液浓度,知道弱酸根离子和弱碱离子相互促进水解,题目难度中等.

练习册系列答案
相关题目
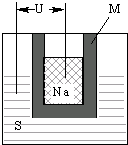 美国福特(Ford)公司于1967年首先发明公布的钠硫电池由于具有高能的诱人特点,受到很多国家极大的重视和发展.图1为钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述正确的是( )
美国福特(Ford)公司于1967年首先发明公布的钠硫电池由于具有高能的诱人特点,受到很多国家极大的重视和发展.图1为钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,该电池的工作温度为320℃左右,电池反应为2Na+xS═Na2Sx,下列叙述正确的是( )| A、M只是用来隔离Na和S |
| B、正极的电极反应式为xS+2e?→Sx2? |
| C、与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的4倍 |
| D、Na+在电池工作过程中朝负极移动 |
下列说法正确的是( )
| A、PM2.5受到普遍的关注,因为PM2.5在空气中形成了气溶胶,富含大量的有毒、有害物质,对空气质量影响较大(PM2.5是指大气中直径接近于2.5×10-6m的颗粒物) |
| B、李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法、元素分析仪都是元素定性分析法 |
| C、泡沫灭火器是最常见的灭火器之一,其内筒为塑料桶,盛有碳酸氢钠溶液;外筒为铁桶,外筒和内筒之间装有硫酸铝溶液 |
| D、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
下列有关电解质溶液的说法正确的是( )
| A、蒸馏水中逐渐加入NaOH(s)的过程中KW不变 |
| B、CaCO3难溶于稀硫酸,更难溶于醋酸 |
| C、在Na2CO3稀溶液中,c(H+)+c(Na+)=c(OH-)+2c(CO32-)+c(HCO3-) |
| D、NaCl溶液和BaCl2溶液中水的KW不同 |
下列解释实验过程或事实的反应方程式不正确的是( )
A、熔融烧碱时,不能使用氧化铝坩埚:Al2O3+2NaOH
| ||||
| B、刻制印刷电路时用FeCl3溶液作为“腐蚀液”:2Fe3++Cu=Cu2++2Fe2+ | ||||
C、打磨后的镁条置于沸水中,滴加酚酞溶液变红色:Mg+2H2O(g)
| ||||
| D、向KI溶液中滴加硫酸酸化的双氧水,溶液呈棕黄色:2I-+H2O2+2H+=I2+O2↑+2H2O |
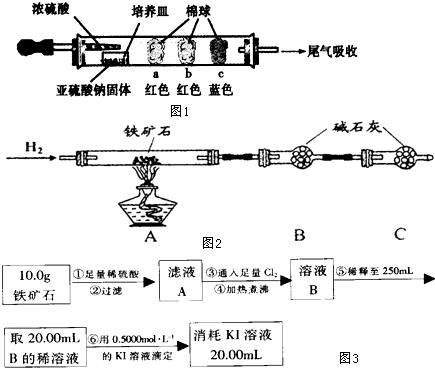
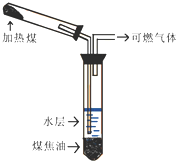 煤的干馏实验如图所示:
煤的干馏实验如图所示: