��Ŀ����
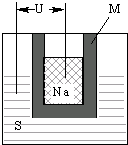 �������أ�Ford����˾��1967�����ȷ������������������ھ��и��ܵ������ص㣬�ܵ��ܶ���Ҽ�������Ӻͷ�չ��ͼ1Ϊ������ܵ�صĽṹʾ��ͼ��M��Na2O��Al2O3�Ƶã��õ�صĹ����¶�Ϊ320�����ң���ط�ӦΪ2Na+xS�TNa2Sx������������ȷ���ǣ�������
�������أ�Ford����˾��1967�����ȷ������������������ھ��и��ܵ������ص㣬�ܵ��ܶ���Ҽ�������Ӻͷ�չ��ͼ1Ϊ������ܵ�صĽṹʾ��ͼ��M��Na2O��Al2O3�Ƶã��õ�صĹ����¶�Ϊ320�����ң���ط�ӦΪ2Na+xS�TNa2Sx������������ȷ���ǣ�������| A��Mֻ����������Na��S |
| B�������ĵ缫��ӦʽΪxS+2e?��Sx2? |
| C����Ǧ������ȣ���������ͬ�����ĸ�����������ʱ�������ص����۷ŵ�����Ǧ���ص�4�� |
| D��Na+�ڵ�ع��������г������ƶ� |
���㣺ԭ��غ͵��صĹ���ԭ��
ר�⣺�绯ѧר��
�������ɷ���ʽ��֪��Ӧ��Na��������ӦΪԭ��ط�����Ӧ���缫����ʽΪNa-e?=Na+��S���ϼ۽��ͣ�����ԭ��Ϊԭ���������Ӧ���缫����ʽΪxS+2e?��Sx2?��ԭ��ع���ʱ��M�������Na��S�����ã��Դ˽����⣮
���
�⣺A������״̬�£�Na2O�ܵ�����������Ӷ�ʹ����ʵ��磬��������Ӧ���������������ã���A����
B����������õ��ӷ�����ԭ��Ӧ�����������缫��ӦʽΪ��xS+2e-�TSx2-����B��ȷ��
C���Ƹ��ܵ���и���Ϊ�ƣ���23g�������ͷ�1mol e-����207g������ʱת��
mol=9mol e-��Ǧ���صĵ缫��ӦΪ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O��Ǧ������Ǧ�Ǹ�����207gǦ����ʱת�� 2mol e-���������ص����۷ŵ�����Ǧ���صģ�9��2=4.5 ������C����
D��ԭ��ع���ʱ���������������ƶ�����D����
��ѡB��
B����������õ��ӷ�����ԭ��Ӧ�����������缫��ӦʽΪ��xS+2e-�TSx2-����B��ȷ��
C���Ƹ��ܵ���и���Ϊ�ƣ���23g�������ͷ�1mol e-����207g������ʱת��
| 207 |
| 23 |
D��ԭ��ع���ʱ���������������ƶ�����D����
��ѡB��
���������⿼����ԭ���ԭ������ȷ�������ϵ�ʧ���Ӽ���Ӧ�����ǽⱾ��ؼ����ѵ��ǵ缫��Ӧʽ����д���״�����A������M���������ȷ��M�ĵ������ã��ѶȺܴ�

��ϰ��ϵ�д�
 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�
�����Ŀ
��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ�������
| A��17g�ǻ���-OH�������еĵ�������10NA�� |
| B��1mol����ϩ�к��е�̼��̼˫����Ϊ4NA�� |
| C�������£�14g��ϩ�ͱ�ϩ�Ļ��������ԭ����Ϊ3NA�� |
| D��4.2g C3H6�к��е�̼̼˫����һ��Ϊ0.1NA |
�ؽᾧ����������ܼ������ʵ��ܽ���٣����л�����ܽ��ԱȽ�ǿ����ôһ�ι��˺�����
| A���л�����Ȼ����Һ�� |
| B����������Һ�� |
| C���л���ͣ������ֽ�� |
| D�����ʡ��л��ﶼͣ�������� |
����˵����ȷ���ǣ�������
| A��������ˮ�еμ�ŨH2SO4��KW���� |
| B��CaCO3������ϡ���ᣬҲ�����ڴ��� |
| C��KClO3��SO3����ˮ���ܵ��磬��KClO3��SO3Ϊ����� |
| D��HCl��Һ�ĵ����Բ�һ��ǿ��CH3COOH��Һ�ĵ����� |
��NAΪ����٤������������˵����ȷ���ǣ�������
| A��NA�������Ӻ�NA������ӵ�������Ϊ8��1 |
| B��11.2L�����к��е�ԭ����ΪNA�� |
| C��54gˮ�к��з�����Ϊ3NA�� |
| D��1mol/L��������Һ�����������������ΪNA |
����˵���У���ȷ���ǣ�������
| A�����������ӵĻ�����һ�����������ӣ����������ӵĻ����ﲻһ������������ |
| B��ֻ����ѧ�������Ӽ��������Ļ����ᄃ��һ����ԭ�Ӿ��� |
| C���������͵���������ͬ����������������һ�ַ��Ӻ�һ������ |
| D��ֻ�з���������ԭ�Ӿ��ﵽ2����8�������ȶ��ṹ�ķ��Ӳ����ȶ����� |
 �����£���100mL 0.01mol?L-1 MOH��Һ����μ���0.02mo1?L-1 HA��Һ��ͼ����ʾ���߱�ʾ�����Һ��pOH�仯�������Һ����仯���Բ��ƣ�����Һ��pOH=-lg��OH-��������˵���У�����ȷ���ǣ�������
�����£���100mL 0.01mol?L-1 MOH��Һ����μ���0.02mo1?L-1 HA��Һ��ͼ����ʾ���߱�ʾ�����Һ��pOH�仯�������Һ����仯���Բ��ƣ�����Һ��pOH=-lg��OH-��������˵���У�����ȷ���ǣ�������| A��HAΪһԪ���� |
| B��MOHΪһԪǿ�� |
| C��N��ˮ�ĵ���̶ȴ���K��ˮ�ĵ���̶� |
| D��K���Ӧ����Һ��pOH=10������c��HA��+c��H+��-c��OH-��=0.01mol?L-1 |
��������ĵ���ƽ�ⳣ�����±���
����ѡ����ȷ���ǣ�������
| ���� | HCOOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� ��25�棩 |
Ka=1.77��10-4 | Ka=4.9��10-10 | Ka1=4.3��10-7 Ka2=5.6��10-11 |
| A��2CN-+H2O+CO2�T2HCN+CO32- |
| B���к͵��������pH��HCOOH��HCN����NaOH����ǰ��С�ں��� |
| C�����ʵ���Ũ����ȵ�HCOONa��KCN��Һ�У�c��Na+��-c��HCOO-����c��K+��-c��CN-�� |
| D��c��NH4+����ȵ�HCOONH4��Һ��NH4CN��Һ��NH4HCO3��Һ�У�c��NH4HCO3����c��NH4CN����c��HCOONH4�� |