题目内容
3. X、Y、Z、W均为短周期元素:在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )
X、Y、Z、W均为短周期元素:在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍.下列说法正确的是( )| A. | X、Y、Z的原子半径大小:X>Y>Z | |
| B. | Y、Z的气态氢化物的热稳定性:Y<Z | |
| C. | Z、W的最高价氧化物对应水化物的酸性:Z<W | |
| D. | X、W的气态氢化物相互反应,生成物中既含离子键又含极性键和非极性键 |
分析 X、Y、Z、W均为短周期元素,由在周期表中位置可知,Y为第二周期元素,Y原子的最外层电子数是其次外层电子数的3倍,则Y的最外层电子数为6,Y为O元素,结合位置可知,X为N,Z为S,W为Cl,以此来解答.
解答 解:由上述分析可知,X为N,Y为O,Z为S,W为Cl,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径大小:Z>X>Y,故A错误;
B.非金属性越强,对应氢化物越稳定,则氢化物的热稳定性:Y>Z,故B错误;
C.非金属性越强,对应最高价含氧酸的酸性越强,则最高价氧化物对应水化物的酸性:Z<W,故C正确;
D.X、W的气态氢化物相互反应生成氯化铵,含离子键、N-H极性键,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,Y为元素推断的突破口,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
14.有关化学用语正确的是( )
| A. | 乙烯的结构简式C2H4 | B. | 乙烷的结构式CH3CH3 | ||
| C. | 四氯化碳的电子式 | D. | 乙酸的分子式C2H4O2 |
18.苯甲醛(C6H5-CHO)在浓NaOH溶液中发生分子间的氧化还原反应,结果一半苯甲醛被氧化,一半苯甲醛被还原.由此判断,最终的反应产物是( )
| A. | 苯甲醇 | B. | 苯甲酸钠 | ||
| C. | 苯甲醇和苯甲酸苯甲酯 | D. | 苯甲醇和苯甲酸钠 |
8.下列金属用热还原法冶炼的是( )
| A. | 钠 | B. | 铁 | C. | 银 | D. | 汞 |
15.某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
下列回答错误的是( )
| 编号 | 电极材料. | 电解质溶液 | 电流计指针 |
| 1 | Mg、Al | 稀盐酸 | 偏转 |
| 2 | Al、Cu | 稀盐酸 | 偏转 |
| 3 | A1、C(石墨) | 稀盐酸 | 偏转 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏转 |
| 5 | Al、Zn | 浓硝酸 | 偏转 |
| A. | 实验1、2中铝所作的电极(正极或负极)不相同 | |
| B. | 实验2、3中,铝电极的电极反应式均为Al-3e-═Al3+ | |
| C. | 实验4中铝电极的电极反应式为:Al-3e-+40H-═A102-+2H2O | |
| D. | 实验5中铝作原电池的负极 |
6.下列表达正确的是( )
| A. | N2的电子式为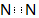 | B. | H2S的电子式可表示为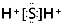 | ||
| C. | 用电子式表示Na2O的形成过程为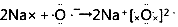 | D. | MgCl2的电子式为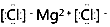 |

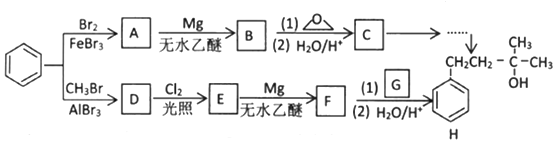
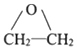 →R-CH2CH2OMgX<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>→H2O/H+$\stackrel{H_{2}O/H+}{→}$R-CH2CH2OH
→R-CH2CH2OMgX<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>→H2O/H+$\stackrel{H_{2}O/H+}{→}$R-CH2CH2OH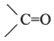 →
→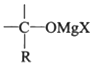 $\stackrel{H_{2}O/H+}{→}$
$\stackrel{H_{2}O/H+}{→}$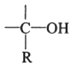
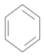 +CH3Br$→_{.}^{AlBr_{3}}$
+CH3Br$→_{.}^{AlBr_{3}}$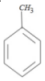 +HBr
+HBr
 ,
,