题目内容
2.把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将所得溶液用石墨电极进行电解,阴极生成的物质是( )| A. | H2 | B. | Ag | C. | Cl2 | D. | O2 |
分析 等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,发生的反应为NaCl+AgNO3=AgCl↓+NaNO3,根据方程式知,NaCl和AgNO3恰好反应生成NaNO3和AgCl,则溶液中溶质为Na2SO4、NaNO3,用石墨作电极电解该混合溶液时,阴极上氢离子放电、阳极上氢氧根离子放电.
解答 解:等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,发生的反应为NaCl+AgNO3=AgCl↓+NaNO3,根据方程式知,NaCl和AgNO3恰好反应生成NaNO3和AgCl,则溶液中溶质为Na2SO4、NaNO3,用石墨作电极电解该混合溶液时,阴极上氢离子放电、阳极上氢氧根离子放电,所以阴极上生成氢气、阳极上生成氧气,
故选A.
点评 本题考查电解原理,为高频考点,正确判断混合溶液中溶质是解本题关键,很多同学往往不考虑物质之间的反应而导致错误,为易错题.

练习册系列答案
相关题目
12.下列溶液中氯离子浓度最小的是( )
| A. | 150ml 1mol/L的NaCl溶液 | B. | 150ml 3mol/LKCl溶液 | ||
| C. | 75ml 2mol/L的NH4Cl溶液 | D. | 50ml 1mol/lCuCl2溶液 |
13.已知热化学方程式:
①C2H2(g)+O2(g)═2CO2(g)+H2O(l)△H1=-1301.0kJ•mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应④2C(s)+H2(g)═C2H2(g)的△H为( )
①C2H2(g)+O2(g)═2CO2(g)+H2O(l)△H1=-1301.0kJ•mol-1
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=-285.8kJ•mol-1
则反应④2C(s)+H2(g)═C2H2(g)的△H为( )
| A. | +228.2 kJ•mol-1 | B. | -228.2 kJ•mol-1 | ||
| C. | +1 301.0 kJ•mol-1 | D. | +621.7 kJ•mol-1 |
10.将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一.一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品.回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
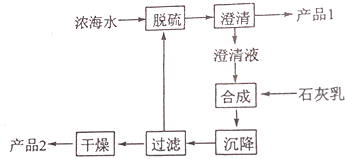
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的离子方程式为Ca2++SO42-=CaSO4↓,产品2的化学式为Mg(OH)2,1L浓海水最多可得到产品2的质量为69.6g.
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.

(1)下列改进和优化海水综合利用工艺的设想和做法可行的是②③④(填序号).
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾.溴.镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收.碱吸收溴的主要反应是:Br2+Na2CO3+H2O→NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为$\frac{5}{3}$mol.
(3)海水提镁的一段工艺流程如图:浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O$\frac{\underline{\;高温\;}}{\;}$Mg(OH)2+H2↑.
17.完成下列表格内容
| 实验操作 | 现象 | 离子方程式 |
| 向澄清石灰水中通入少量CO2气体 | ||
| 向硫酸溶液中投入少量Mg粉 | ||
| 向醋酸溶液中滴加NaOH溶液 | 无明显现象 |
7.PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生反应:PCl3(g)+Cl2(g)?PCl5(g),并于10min时达到平衡.有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol•L-1•min-1 | |
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol•L-1 |
14.同温同压下,分子数相同的氨气和氢气,它们( )
| A. | 所占的体积相同 | B. | 密度相同 | ||
| C. | 所含原子数目相同 | D. | 所占体积一定是22.4L |
 实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有:
实验室配制500mL、0.2mol/L的Na2SO4溶液,实验操作步骤有: 如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的数据,请根据有关数据回答下列问题: