题目内容
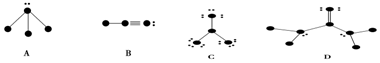
20.砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )| A. | 黄砷中共价键键能大于白磷 | B. | 黄砷的熔点高于白磷 | ||
| C. | 黄砷易溶于水 | D. | 分子中共价键键角均为109°28′ |
分析 As和P位于相同主族,原子半径As>P,由同主族元素从上到下非金属性逐渐减弱可知非金属性P>As,形成的晶体都为分子晶体,相对分子质量越大,分子间作用力越强,以此解答.
解答 解:A.原子半径As>P,键长越大键能越小,则黄砷中共价键键能小于白磷,故A错误;
B.二者形成的晶体都为分子晶体,相对分子质量越大,分子间作用力越强,熔点越高,则黄砷的熔点高于白磷,故B正确;
C.黄砷为非极性分子,水为极性溶剂,根据相似相溶原理,黄砷不易溶于水,故C错误;
D.P4、As4都为正四面体结构,As、P原子位于正四面体的顶点上,分子中共价键键角均为60°,故D错误.
故选B.
点评 本题考查同主族元素的性质的递变规律、物质结构与性质等,侧重于学生的分析能力和基本概念的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
8.短周期主族元素X、Y、Z、W的原子序数依次增大,X的氢化物极易溶于Y的氢化物中,常温下Z的单质能溶于X的最高价氧化物对应的水化物的稀溶液中,不溶于其浓溶液中,W元素的最高正价与最低负价代数和为+4,下列说法正确的是( )
| A. | 钠与W可以形成Na2W2化合物 | |
| B. | Z与少量的氢氧化钠溶液反应生成两性氢氧化物 | |
| C. | X与氢元素只能形成含共价键的化合物 | |
| D. | WO2与XO2均为酸性氧化物 |
15.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 碳棒作电极电解饱和食盐水,阳极的电极反应式为2Cl--2e-═Cl2↑ | |
| B. | 由C(石墨)(s)═C(金刚石)(s)△H=+1.90 kJ•mol-1可知,金刚石比石墨稳定 | |
| C. | 粗铜精炼时,与电池正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3KJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时也放出57.3 kJ的热量 |
12.下列关于能源的叙述错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 氢氧燃料电池工作过程中,热能转变为电能 | |
| C. | 电解水制取H2过程中,电能转变为化学能 | |
| D. | 生物质能源是可再生能源 |
9.(1)MgCl2•6H2O晶体受热水解可以生成MgOHCl,但产率较低,其化学方程式为MgCl2•6 H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+HCl↑+5 H2O.
I.先用空气得到氮气,可供选择的装置和药品如图1(还原铁粉已干燥,装置内发生的反应是完全的).
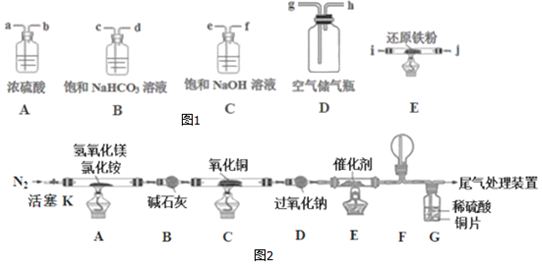
(2)连接并检查装置的气密性.实验开始时,打开自来水的开关,将空气从5L的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)h→e→f→a→b→i→j.
II.将得到的氮气通入如图装置参与制备碱式氯化镁并探究氨的催化氧化反应(其中CuO的质量为8.0g).
(3)装置A中发生反应生成碱式氯化镁的化学方程为Mg(OH)2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+NH3↑+H2O.
(4)实验结束时进行正确操作是C.
A.关闭活塞K,先熄灭A处酒精灯,后熄灭C、E处酒精灯
B.先熄灭A处酒精灯,关闭活塞K,后熄灭C、E处酒精灯
C.先熄灭A处酒精灯,再熄灭C、E处酒精灯,后关闭活塞K
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,甲同学设计一个实验方案,证明装置C中完全反应后的红色固体中含Cu2O.己知:①Cu2O+H+═Cu2++Cu;②限选试剂:2mol/L H2SO4溶液、12mol/L H2SO4溶液、2mol/L HNO3溶液、10mol/L HNO3溶液.
乙同学称量C中红色物质,质量为6.8g,且生成的气体可直接排放到大气中,进一步确定红色固体是Cu和Cu2O,该反应中电子转移的物质的量为0.15mol.
I.先用空气得到氮气,可供选择的装置和药品如图1(还原铁粉已干燥,装置内发生的反应是完全的).

(2)连接并检查装置的气密性.实验开始时,打开自来水的开关,将空气从5L的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)h→e→f→a→b→i→j.
II.将得到的氮气通入如图装置参与制备碱式氯化镁并探究氨的催化氧化反应(其中CuO的质量为8.0g).
(3)装置A中发生反应生成碱式氯化镁的化学方程为Mg(OH)2+NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$MgOHCl+NH3↑+H2O.
(4)实验结束时进行正确操作是C.
A.关闭活塞K,先熄灭A处酒精灯,后熄灭C、E处酒精灯
B.先熄灭A处酒精灯,关闭活塞K,后熄灭C、E处酒精灯
C.先熄灭A处酒精灯,再熄灭C、E处酒精灯,后关闭活塞K
(5)反应完毕,装置C中的氧化铜完全反应,由黑色变为红色,甲同学设计一个实验方案,证明装置C中完全反应后的红色固体中含Cu2O.己知:①Cu2O+H+═Cu2++Cu;②限选试剂:2mol/L H2SO4溶液、12mol/L H2SO4溶液、2mol/L HNO3溶液、10mol/L HNO3溶液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取装置C中反应后的少许固体于试管中 | |
| 步骤2: 向试管中加入2mol/LH2SO4溶液 | 溶液中出现蓝色,说明红色固体中含有Cu2O,Cu和Cu2O |
15.如图所示的实验操作不正确的是( )
| A. |  铁丝在氧气中燃烧 | B. |  读取液体的体积 | ||
| C. |  除去CO中的CO2 | D. |  制取蒸馏水 |
 D在周期表的位置:第三周期VIIA族.
D在周期表的位置:第三周期VIIA族. .
.
 .
.