题目内容
7.锂电池具有高能量、寿命长、可靠性高等优点,即使是在非常低的温度下作业也能有出色的表现.某种锂电池的总反应为Li+MnO2═LiMnO2,下列说法不正确的是( )| A. | Li是负极,电极反应为Li-e-═Li+ | |
| B. | 锂电池属于一次性电池 | |
| C. | MnO2是正极,电极反应为MnO2+e-═MnO${\;}_{2}^{-}$ | |
| D. | 锂电池是一种环保型电池 |
分析 根据电池反应式知,Li失电子发生氧化反应,则Li作负极、MnO2作氧化剂,负极反应式为Li-e-═Li+、正极反应式为MnO2+e-═MnO2-,据此分析解答.
解答 解:A.根据电池反应式知,Li失电子发生氧化反应,则Li作负极、电极反应式为:Li-e-═Li+,故A正确;
B.锂电池是可充可放的电池,属于二次性电池,故B错误;
C.MnO2为正极,发生反应MnO2+e-═MnO2-,故C正确;
D.锂电池无污染,是一种环保型电池,故D正确;
故选B.
点评 本题考查原电池原理,明确元素化合价升降与电极关系是解本题关键,电极反应式书写是学习难点,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
20.表是元素周期表的一部分,针对表中①~⑩种元素,填写下列空白:
(1)被选作相对原子质量标准的核素是12C(填核素符号).
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素其单质与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(4)从⑤到⑧的元素中,Al3+离子半径最小(填离子符号).
(5)元素③与⑤形成的具有强氧化性的化合物的电子式 .
.
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A.将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B.比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C.将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D.将⑤、⑥的单质分别在O2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素其单质与氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(4)从⑤到⑧的元素中,Al3+离子半径最小(填离子符号).
(5)元素③与⑤形成的具有强氧化性的化合物的电子式
 .
.(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A.将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B.比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C.将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D.将⑤、⑥的单质分别在O2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
17.离子方程式H++OH-═H2O所表示的反应是( )
| A. | 所有酸和碱之间的中和反应 | |
| B. | 所有强酸和强碱之间的中和反应 | |
| C. | 所有可溶性酸和可溶性碱之间的中和反应 | |
| D. | 强酸溶液与强碱溶液生成可溶性盐和水的反应 |
2.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑩十种元素在周期表中的位置.
(1)在这十种元素中,化学性质最不活泼的元素是氩 (填元素名称),金属性最强的元素符号是Mg (填元素符号),元素④的离子结构示意图是 ,①⑥⑦中原子半径最小的是C (填元素符号).
,①⑥⑦中原子半径最小的是C (填元素符号).
(2)元素④和⑨的气态氢化物中较稳定的物质是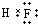 (填电子式)
(填电子式)
(3)⑤和⑨能以离子 (填化学键类型)键结合形成离子 (填晶体类型)晶体,溶解时破坏离子键 (填作用力类型).
(4)⑧和⑨离子的还原性比较⑧大于 ⑨(填大于、小于),最高价氧化物对应水化物的酸性更强的物质是HClO4 (填化学式)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | =10 ⑩ |
 ,①⑥⑦中原子半径最小的是C (填元素符号).
,①⑥⑦中原子半径最小的是C (填元素符号).(2)元素④和⑨的气态氢化物中较稳定的物质是
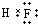 (填电子式)
(填电子式)(3)⑤和⑨能以离子 (填化学键类型)键结合形成离子 (填晶体类型)晶体,溶解时破坏离子键 (填作用力类型).
(4)⑧和⑨离子的还原性比较⑧大于 ⑨(填大于、小于),最高价氧化物对应水化物的酸性更强的物质是HClO4 (填化学式)
19.运用下列装置和操作能达到实验目的和要求的是( )
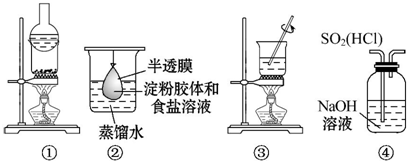

| A. | 用①分离氯化铵和单质碘 | |
| B. | 用②除去淀粉溶液中的氯化钠 | |
| C. | 用③加热胆矾(CuSO4•5H2O)制取无水硫酸铜 | |
| D. | 用④装置除去SO2中的HCl |
16.用铝热法还原下列化合物,当各制得1mol金属单质时,消耗铝的质量最少的是( )
| A. | WO3 | B. | Fe3O4 | C. | MnO2 | D. | V2O5 |
17.用下列实验装置进行的实验中,能达到相应实验目的是( )
| A. | 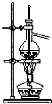 海水蒸馏 | B. | 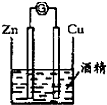 形成原电池 | C. | 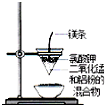 可制得金属锰 | D. | 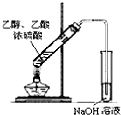 制取乙酸乙酯 |

 天然气的主要成分甲烷燃烧生成二氧化碳和液态水的化学方程式是:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-889.6kJ/mol
天然气的主要成分甲烷燃烧生成二氧化碳和液态水的化学方程式是:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H═-889.6kJ/mol