题目内容
19.在如图装置中,Zn为负极,Zn电极反应式为Zn-2e-=Zn2+,Cu电极的电极反应式为2H++2e-=H2↑;
分析 该装置构成原电池,Zn易失电子作负极、Cu作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应.
解答 解:该装置构成原电池,Zn易失电子作负极、Cu作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,负极反应式为Zn-2e-=Zn2+,正极反应式为2H++2e-=H2↑,故答案为:负;Zn-2e-=Zn2+;2H++2e-=H2↑.
点评 本题以电极反应式的书写为载体考查原电池原理,为高频考点,明确各个电极上发生的反应及反应类型、电子转移是解本题关键,注意结合电解质溶液特点书写电极反应式.

练习册系列答案
相关题目
9.下列化学用语正确的是( )
| A. | K+的结构示意图: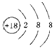 | B. | 四氯化碳的电子式: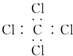 | ||
| C. | CH4分子的比例模型: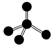 | D. | 过氧化氢结构式:H-O-O-H |
7.华裔科学家高琨因“在光导纤维传输信息领域中的突破性成就”获得2009年诺贝尔物理学奖,下列有关硅材料的说法正确的是( )
| A. | 光导纤维的主要成分是高纯度的单质硅 | |
| B. | 硅在地壳中的含量仅次于氧,自然界中存在大量单质硅 | |
| C. | 硅的化学性质不活泼,常温下不与任何物质起反应 | |
| D. | 硅同素异形体有晶体硅和无定形硅,晶体硅是灰黑色有金属光泽的固体 |
4.下列描叙中,正确的是( )
| A. | Cl2以液态形式存在时可称作氯水或液氯 | |
| B. | 玛瑙的主要成分是二氧化硅 | |
| C. | 加碘食盐中所加的“碘”是KIO3 | |
| D. | 漂白粉的主要成分是次氯酸钙 |
11.下列有关物质的性质与应用的对应关系正确的是( )
| A. | ClO2具有强还原性,可用于自来水的杀菌消毒 | |
| B. | 晶体硅具有导电性,可用于制作光导纤维 | |
| C. | MgO的熔点很高,可用于制作耐高温材料 | |
| D. | 浓硫酸具有吸水性,可用于干燥氯气、氨气等气体 |
8.下列离子反应方程式正确的是( )
| A. | Na2O2与水反应:2O22-+2H2O═4OH-+O2↑ | |
| B. | 小苏打与烧碱溶液反应 HCO3-+OH-═CO2↑+H2O | |
| C. | Ca(HCO3)2与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ |
7.锂电池具有高能量、寿命长、可靠性高等优点,即使是在非常低的温度下作业也能有出色的表现.某种锂电池的总反应为Li+MnO2═LiMnO2,下列说法不正确的是( )
| A. | Li是负极,电极反应为Li-e-═Li+ | |
| B. | 锂电池属于一次性电池 | |
| C. | MnO2是正极,电极反应为MnO2+e-═MnO${\;}_{2}^{-}$ | |
| D. | 锂电池是一种环保型电池 |
