题目内容
18.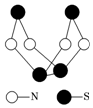 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
分析 由图可知,分子中含4个N原子、4个S原子,只含存在共价键,为分子晶体,以此来解答.
解答 解:A.化合物分子式为S4N4,故A错误;
B.只存在S-N共价键,故B正确;
C.为分子晶体,熔沸点较低,故C错误;
D.该物质与化合物S2N2,均为化合物,为不同的物质,故D错误;
故选B.
点评 本题考查物质的结构,为高频考点,把握分子式、化学键及晶体类型为解答的关键,侧重分析与应用能力的考查,注意同素异形体的分析对象为单质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.在使酚酞变红的溶液中,能大量共存的离子组是( )
| A. | Na+ HCO3- SO42- Br- | B. | Cu2+ K+ SO42- NO3- | ||
| C. | Na+ K+ Cl- NO3- | D. | Fe3+ K+ SO42- Cl- |
13.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-Q1KJ•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-$\frac{1}{2}$Q2•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-$\frac{1}{2}$Q3•mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量(单位:KJ)为( )
H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-$\frac{1}{2}$Q2•mol-1
H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-$\frac{1}{2}$Q3•mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量(单位:KJ)为( )
| A. | 0.4Q1+0.05Q3 | B. | 0.4Q1+0.05Q2 | C. | 0.4Q1+0.1Q3 | D. | 0.4Q1+0.2Q2 |
3.针对下面10种元素,完成以下各小题.
(1)地壳中含量最多的元素是氧(或氧元素)(填名称).
(2)最高价氧化物对应的水化物碱性最强的是NaOH(填化学式).
(3)Al的原子结构示意图为 .
.
(4)S和Cl相比,元素非金属性较强的是Cl.
(5)可用来制造光导纤维的物质是二氧化硅(或SiO2),晶体硅的主要用途是制造半导体材料(写出一种).
(6)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)最高价氧化物对应的水化物碱性最强的是NaOH(填化学式).
(3)Al的原子结构示意图为
 .
.(4)S和Cl相比,元素非金属性较强的是Cl.
(5)可用来制造光导纤维的物质是二氧化硅(或SiO2),晶体硅的主要用途是制造半导体材料(写出一种).
(6)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
10.下列化合物的核磁共振氢谱中出现三个峰的是( )
| A. | 2,5-二甲基己烷 | B. | 2,2-二甲基丙烷 | ||
| C. | 2,6-二甲基庚烷 | D. | 2,2,3,3-四甲基丁烷 |

