题目内容
6.某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如图.有一种气体是红棕色.请回答下列问题:
(1)溶液X中除了H+一定存在的离子有Al3+、NH4+、Fe2+、SO42-.溶液X中一定不存在的离子有Ba2+、CO32-、SiO32-、NO3-.
(2)产生气体A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO+2H2O.
(3)转化⑥发生反应的现象为红褐色沉淀溶解,溶液呈黄色.
(4)转化 ⑤中的离子方程式为NH3+H+═NH4+.
(5)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中O2与D的物质的量之比为1:4.
分析 某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;
酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,气体A是NO,由反应②可知生成D为NO2,③中生成E为硝酸;
溶液B中加入过量氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,由于溶液中存在Fe2+,沉淀G是Fe(OH)3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,溶液H中含有偏铝酸根,沉淀K是Al(OH)3,溶液L是NaHCO3,以此来解答.
解答 解:某强酸性溶液X,则溶液中不存在弱酸根离子CO32-、SiO32-,溶液和硝酸钡溶液反应生成沉淀C,则溶液存在SO42-,不存在和硫酸根离子反应的Ba2+,C是BaSO4;
酸性条件下硝酸根离子具有强氧化性,所以溶液中Fe2+和NO3-不能共存,加入硝酸钡产生气体,则溶液中存在Fe2+,不存在NO3-,气体A是NO,由反应②可知生成D为NO2,③中生成E为硝酸;
溶液B中加入过量氢氧化钠溶液时,产生气体F,则溶液中含有NH4+,F是NH3,产生沉淀,由于溶液中存在Fe2+,沉淀G是Fe(OH)3,溶液H中通入过量二氧化碳生成沉淀,则溶液中存在Al3+,溶液H中含有偏铝酸根,沉淀K是Al(OH)3,溶液L是NaHCO3;
(1)综上所述,溶液X中除H+外肯定含有的离子是Al3+、SO42-、NH4+、Fe2+;不能确定是否含有的离子Fe3+,一定不存在的离子为Ba2+、CO32-、SiO32-、NO3-,
故答案为:Al3+、SO42-、NH4+、Fe2+;Ba2+、CO32-、SiO32-、NO3-;
(2)产生气体A的离子方程式为3Fe2++NO3-+4H+=3Fe3++NO+2H2O,故答案为:3Fe2++NO3-+4H+=3Fe3++NO+2H2O;
(3)转化⑥中Fe(OH)3与盐酸反应生成氯化铁,发生反应的现象为红褐色沉淀溶解,溶液呈黄色,故答案为:红褐色沉淀溶解,溶液呈黄色;
(4)转化⑤中的离子方程式为NH3+H+═NH4+,故答案为:NH3+H+═NH4+;
(5)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,发生4NO2+O2+2H2O=4HNO3,则反应中O2与D的物质的量之比为1:4,故答案为:1:4.
点评 本题考查常见离子的检验,为高频考点,把握离子的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意发生的氧化还原反应,题目难度不大.

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案| A. | 氢氧化镁和稀盐酸反应 | B. | Ba(OH)2溶液滴入稀硫酸中 | ||
| C. | 澄清石灰水和稀硝酸反应 | D. | CH3COOH溶液和NaOH溶液反应 |
①点燃氢气前要检验氢气的纯度,以免发生爆炸;
②CO气体有毒,处理CO气体时可将其点燃,转化为无毒的CO2;
③在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子;
④用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ①③④ |
| A. | BeCl2 | B. | H2S | C. | PCl3 | D. | SF4 |
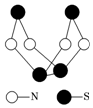 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 5 | 5 | 55 | 5 |
| 反应后质量/g | 27 | 待测 | 0 | 19 |
| A. | a% | B. | 2a% | C. | 100%-1.75a% | D. | 100%-0.75a% |