题目内容
下列实验操作中,错误的是
A. 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B. 蒸馏时,应使温度计水银球位于蒸馏烧瓶支管口处
C. 用酒精萃取碘水溶液中的碘
D. 过滤时漏斗下端尖嘴应与烧杯内壁紧靠
练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
18.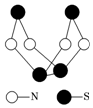 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
19.运用元素周期律分析下面的推断不正确的是( )
| A. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| B. | 砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 | |
| C. | 硫酸锶难溶于水,但易溶于盐酸 | |
| D. | 硒化氢是无色、有毒、比硫化氢稳定的气体 |
16.由硫氢化钠、硫酸镁和亚硫酸氢钠组成的混合物中硫元素的质量分数为a%,该混合物中氧元素的质量分数为( )
| A. | a% | B. | 2a% | C. | 100%-1.75a% | D. | 100%-0.75a% |
2.根据下列信息试回答下列问题
(Ⅰ)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
①该反应的△H<0,△S(熵变)<0,(填“>”、“<”或“=”).
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则此时的温度为250℃;以CH3OH表示该过程的反应速率:v(CH3OH)=0.08mol/(L.min).
(2)图3表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A< C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
(Ⅱ)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2,在500℃下发生发应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).
实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图1所示:

(1)从反应开始到10min达到平衡,氢气的平均反应速率v(H2)=0.225mol/(L•min).500℃达平衡时,CH3OH(g)的体积分数为30%.
(2)图2是改变温度时化学反应速率随时间变化的示意图,则该反应的正反应为放热反应(填“放热”或“吸热”).
(3)下列措施中不能使CO2的转化率增大的是BD.
A.在原容器中再充入1mol H2 B.在原容器中再充入1molCO2
C.缩小容器的容积 D.使用更有效的催化剂.
(Ⅰ)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
(1)下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则此时的温度为250℃;以CH3OH表示该过程的反应速率:v(CH3OH)=0.08mol/(L.min).
(2)图3表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A< C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
(Ⅱ)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.目前工业上有一种方法是用CO2来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2,在500℃下发生发应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g).
实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图1所示:

(1)从反应开始到10min达到平衡,氢气的平均反应速率v(H2)=0.225mol/(L•min).500℃达平衡时,CH3OH(g)的体积分数为30%.
(2)图2是改变温度时化学反应速率随时间变化的示意图,则该反应的正反应为放热反应(填“放热”或“吸热”).
(3)下列措施中不能使CO2的转化率增大的是BD.
A.在原容器中再充入1mol H2 B.在原容器中再充入1molCO2
C.缩小容器的容积 D.使用更有效的催化剂.


 含的分子个数
含的分子个数