题目内容
10.某有机物结构如图,它不可能具有的性质是( )
| A. | 能跟KOH溶液反应 | B. | 能被氧化 | C. | 能发生加聚反应 | D. | 能使溴水褪色 |
分析 由结构可知,分子中含碳碳双键、-OH,结合烯烃、醇的性质来解答.
解答 解:A.不含-COOH、酚-OH、-COOC-、-X等,则不能与KOH溶液反应,故A错误;
B.含碳碳双键、-OH,能被氧化,故B正确;
C.含碳碳双键,能发生加聚反应,故C正确;
D.含碳碳双键,能使溴水褪色,发生加成反应,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意酚与醇的区别及酚、烯烃的性质,题目难度不大.

练习册系列答案
相关题目
20.室温下,H2+Cl2$\stackrel{点燃}{→}$2HCl 生成 0.1mol HCl,下列说法正确的是( )
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
1.根据要求回答下列问题
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种
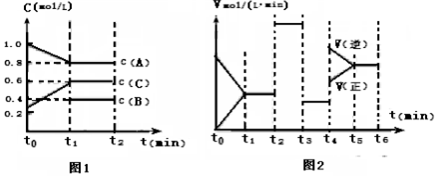
①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
K2> K4(填“>或<或.=”);其理由是t2-t4 平衡未移动,从图象知K4是温度升高平衡逆向移动后的常数,所以变小
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
(1)T0C时,向一容积为2升的密闭容器中充入2molA、0.6molC和一定量的B三种气体,一定条件下发生反应.其相关信息如下:图1中t0~t1阶段c(B)未画出;图2中t2、t3、t4改变的条件是温度、压强、催化剂中的一种

①B的起始物质的量为1mol;t2时刻改变的条件是加催化剂
②图2中各阶段平衡时对应的平衡常数如表所示:
| 时间段 | t1~t2 | t2~t3 | t3~t4 | t5~t6 |
| 平衡常数 | K1 | K2 | K3 | K4 |
③T0C时,该反应的平衡常数是0.84(保留两位小数);维持温度不变,在t1时刻再向该容器中加入1molA,0.5molB,0.3molC,重新达平衡后α(A)=20%
(2)硅是重要的半导体材料.工业上由粗制纯硅的过程如下:
Si(粗)$→_{460℃}^{Cl_{2}}$SiCl4$\stackrel{蒸馏}{→}$SiCl4(纯)$→_{1100℃}^{H_{2}}$Si(纯)
实验测得上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅(Si的相对原子质量为28)需吸收aKJ热量,则该反应的热化学方程式SiCl4(g)+2H2(g)=Si(s)+4HCl(g)△=+Q/40 KJ/mol.
18.中华民族有着光辉灿烂的发明史,下列发明创造的主要原理不涉及化学变化的是( )
| A. | 黑火药的使用 | B. | 用铁矿石炼铁 | ||
| C. | 打磨磁石制备指南针 | D. | 造纸术的使用 |
5.某有机物的结构简式如图所示,关于该物质的叙述错误的是( )
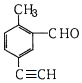

| A. | 能使酸性KMnO4溶液褪色 | |
| B. | 与新制氢氧化铜悬浊液加热煮沸产生砖红色沉淀 | |
| C. | 1mol该物质和H2反应,最多消耗5molH2 | |
| D. | 苯环上的一氯代物有3种 |
15.将浓度均为0.2mol/L的CH3COOH和CH3COONa溶液等体积混合,混合液呈弱酸性,其中有三种微粒的浓度非常接近,这三种微粒是( )
| A. | CH3COO- Na+ CH3COOH | B. | CH3COO- CH3COOH H+ | ||
| C. | CH3COOH OH- H+ | D. | CH3COO- OH- H+ |
2.除去FeCl2溶液中的FeCl3所需试剂是( )
| A. | Cl2 | B. | Cu | C. | Fe | D. | NaOH |
19.pH与体积都相同的硫酸和醋酸溶液,分别与同物质的量浓度、同体积的Na2CO3溶液反应,若在相同条件下放出CO2的量相同,则下列推断合理的是( )
| A. | Na2CO3过量 | B. | Na2CO3恰好与醋酸完全反应 | ||
| C. | 两种酸都过量 | D. | 两种酸的物质的量浓度相同 |
20.下列元素位于d区的是( )
| A. | C | B. | Ca | C. | Cr | D. | Ga |