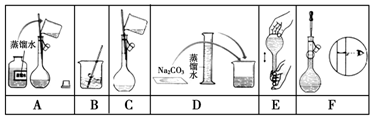
题目内容
5.二价铬不稳定,极易被氧气氧化.醋酸亚铬水合物{[Cr(CH3COO)2]2•2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水和醚,易溶于盐酸,是常用的氧气吸收剂.实验室中以锌粒、CrCl3溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,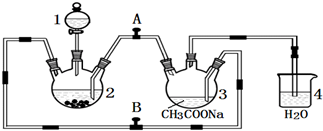
制备过程中发生的反应如下:
Zn(s)+2HCl(aq)═ZnCl2(aq)+H2(g);
2CrCl3(aq)+Zn(s)═2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)=[Cr(CH3COO)2]2•2H2O (s)
请回答下列问题:(1)仪器1的名称是分液漏斗,所盛装的试剂是盐酸.
(2)本实验中所用的溶液,配制用的蒸馏水都需事先煮沸,原因是去除水中的溶解氧,防止Cr2+被氧化.
(3)装置4的主要作用是防止空气进入装置3.
(4)实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应打开阀门A关闭阀门B(填“打开”或“关闭”).
(5)本实验中锌粒须过量,其原因是与CrCl3充分反应得到CrCl2;产生足量的H2,将CrCl2溶液压入装置3与CH3COONa溶液反应.
(6)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质6.34g,实验后得干燥纯净的[Cr(CH3COO)2]2•2H2O 5.64g,则该实验所得产品的产率为75%.
分析 (1)依据装置图形状和作用分析,仪器1为分液漏斗,盛装稀盐酸;
(2)配制用的蒸馏水都需事先煮沸,防止氧气氧化Cr2+;
(3)装置4是保持装置压强平衡,同时避免空气进入;
(4)实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开A关闭B,把生成的CrCl2溶液压入装置3中反应;
(5)锌的作用是和盐酸反应生成氢气,增大仪器中的压强把生成的CrCl2溶液压入装置3,与CrCl3充分反应得到CrCl2;
(6)依据化学方程式定量关系计算分析,产率=$\frac{实际产量}{理论产量}$×100%.
解答 解:(1)根据仪器1的构造可知其名称为分液漏斗,盛装的稀盐酸与锌反应生成氢气,用来增大压强把生成的CrCl2溶液压入装置3中,
故答案为:分液漏斗;盐酸;
(2)由于二价铬不稳定,极易被氧气氧化,需要将配制用的蒸馏水事先煮沸,去除水中的溶解氧,防止Cr2+被氧化,
故答案为:去除水中的溶解氧,防止Cr2+被氧化;
(3)二价铬不稳定,极易被氧气氧化,装置4的主要作用是防止空气进入装置3,
故答案为:防止空气进入装置3;
(4)实验开始生成H2气后,为使生成的CrCl2溶液与CH3COONa溶液顺利混合,打开A关闭B,把生成的CrCl2溶液压入装置3中反应,
故答案为:打开;关闭;
(5)锌的作用是和盐酸反应生成氢气,增大仪器中的压强把生成的CrCl2溶液压入装置3,与CrCl3充分反应得到CrCl2,
故答案为:与CrCl3充分反应得到CrCl2; 产生足量的H2,将CrCl2溶液压入装置3与CH3COONa溶液反应;
(6)实验时取用的CrCl3溶液中含溶质6.34g,
理论上得到[Cr(CH3COO)2]2•2H2O 的质量为:$\frac{6.34g}{158.5g/mol}$×$\frac{1}{2}$×376g/mol=7.52g,
则该实验所得产品的产率为:$\frac{5.64g}{7.52g}$×100%=75%,
故答案为:75%.
点评 本题考查了物质制备实验装置分析判断,实验设计方法和物质性质的理解应用,主要是实验原理的分析应用,掌握基础是关键,题目难度中等,明确实验目的、实验原理为解答关键.

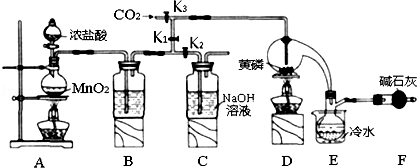
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和HC1;
③PCl3遇O2会生成P0Cl3,P0Cl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)装置F的名称是干燥管,其中装的碱石灰的作用是吸收多余的氯气、防止空气中的H2O进入烧瓶和PCl3 反应;
(3)实验时,检査装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃;
(4)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3;
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O;
(6)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol•L-1碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol•L-1的Na2S2O3,溶液滴定;
③重复②、③操作,平均消耗Na2S2O3溶液8.40ml.
已知:H3PO3+H2O+I2═H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,假设测定过程中没有其他反应,根据上述数据,该产品中PC13的质量分数为79.75%.
 苯甲醛(
苯甲醛(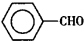 )、苯甲酸(
)、苯甲酸(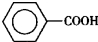 )都是重要的化工原料,都可用甲苯(
)都是重要的化工原料,都可用甲苯(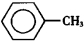 )为原料生产.下表列出了有关物质的部分物理性质,请回答:
)为原料生产.下表列出了有关物质的部分物理性质,请回答:| 名称 | 性状 | 熔点(℃) | 沸点(℃) | 相对密度 ρ水=1g/cm3 | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8660 | 不溶 | 互溶 |
| 苯甲醛 | 无色液体 | -26 | 179 | 1.0440 | 微溶 | 互溶 |
| 苯甲酸 | 白色片状或针状晶体 | 122.1 | 249 | 1.2659 | 微溶 | 易溶 |
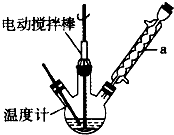
实验室可用如图装置模拟制备苯甲醛.实验时先在三颈瓶中加入0.5g固态难溶性催化剂,再加入15mL冰醋酸和
2mL甲苯,搅拌升温至70℃,同时缓慢加入12mL过氧化氢,在此温度下搅拌反应3小时.
(1)仪器a的主要作用是冷凝回流,防止甲苯挥发导致产率降低.三颈瓶中发生反应的化学方程式为
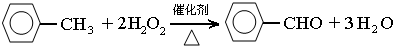 .
.(2)经测定,反应温度升高时,甲苯的转化率逐渐增大,但温度过高时,苯甲醛的产量却有所减少,可能的原因是温度过高时过氧化氢分解速度加快,实际参加反应的过氧化氢质量减小,影响产量.
(3)反应完毕后,反应混合液经过自然冷却至室温时,还应经过过滤、蒸馏(填操作名称)等操作,才能得到苯甲醛粗产品.
(4)实验中加入过量的过氧化氢并延长反应时间时,会使苯甲醛产品中产生较多的苯甲酸.
①若想从混有苯甲酸的苯甲醛中分离出苯甲酸,正确的操作步骤是dacb(按步骤顺序填字母).
a.对混合液进行分液 b.过滤、洗涤、干燥
c.水层中加人盐酸调节pH=2 d.与适量碳酸氢钠溶液混合振荡
②若对实验①中获得的苯甲酸产品进行纯度测定,可称取2.500g产品,溶于100mL乙醇配成溶液,量取所得的乙醇溶液10.00mL于锥形瓶,滴加2~3滴酚酞指示剂,然后用预先配好的0.1000mol/LKOH标准液滴定,到达滴定终点时消耗KOH溶液20.00mL.产品中苯甲酸的质量分数为97.60%.下列情况会使测定结果偏低的是ad(填字母).
a.滴定时俯视读取耗碱量 b.碱式滴定管用蒸馏水洗净后即盛装KOH标准液
c.配制KOH标准液时仰视定容 d.将酚酞指示剂换为甲基橙溶液.
| A. | HF电离:HF(aq)?H+(aq)+F-(aq)△H=+10.4kJ/mol | |
| B. | 水解消耗0.1mol F-时,吸收的热量为6.77kJ | |
| C. | 中和热均为57.3 kJ/mol | |
| D. | 含0.1mol HF、0.1mol NaOH 的两种溶液混合后放出的热量为6.77kJ |