题目内容
20.下列叙述正确的是( )| A. | 离子晶体中一定含有离子键 | |
| B. | 分子晶体中一定含有共价键 | |
| C. | 氧化钠和过氧化钠中含有的化学键种类相同 | |
| D. | 通常情况下水分子较稳定,是因为水分子间存在氢键 |
分析 A.含有离子键的晶体是离子晶体,离子晶体中可能含有共价键;
B.分子晶体中可能只含分子间作用力而不存在化学键;
C.过氧化钠中含有离子键和非极性键,氧化钠中只存在离子键;
D.物质的稳定性与化学键有关,与分子间作用力无关.
解答 解:A.含有离子键的晶体是离子晶体,所以离子晶体中一定含有离子键,离子晶体中可能含有共价键,如KOH,故A正确;
B.分子晶体中可能只含分子间作用力而不存在化学键,如稀有气体,故B错误;
C.过氧化钠中含有离子键和非极性键,氧化钠中只存在离子键,所以二者含有化学键类型不同,故C错误;
D.物质的稳定性与化学键有关,与分子间作用力无关,所以水分子稳定性与氢键无关,氢键影响其熔沸点,故D错误;
故选A.
点评 本题考查化学键判断,侧重考查基本概念,明确物质构成微粒及微粒之间作用力即可解答,采用举例法分析解答,注意规律中的异常现象,易错选项是BD.

练习册系列答案
相关题目
11.下表为元素周期表短周期的一部分,下列有关X、Y、Z、W四种元素的叙述正确的是( )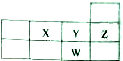

| A. | 原子半径大小:W>Y>X | B. | 核电荷数:W>Z>Y>X | ||
| C. | W的氧化物对应的水化物为强酸 | D. | X是ⅥA族元素,其最高化合价为+6价 |
8.某课外活动小组使用下图装置利用浓盐酸制取氯气并制备一定量的FeCl3,下列说法错误的是( )

| A. | 装置a烧瓶内加入的固体可以是MnO2 | |
| B. | 若按a、e、d、b、c顺序连接装置,则e中盛装的是浓硫酸 | |
| C. | 制备过程中装置b硬质玻璃管内有红棕色的烟产生 | |
| D. | 验证产物中的Fe3+存在可使用KSCN溶液 |
15.下列说法正确的是( )
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5 | |
| C. | 氯化氢的沸点比溴化氢的沸点高 | |
| D. | Li、Na、K单质的熔点逐渐升高 |
5.将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示.下列说法错误的是( )
体积分数/% 压强/MPa 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1 000 | e | f | 83.0 |
| A. | a<54.0 | B. | b>f | ||
| C. | 915℃,2.0 MPa时E的转化率为60% | D. | K(1000℃)>K(810℃) |
12.下列离子在溶液中可以大量共存的一组是( )
| A. | Na+ NO3- SO42- | B. | Ag+ NO3- Cl- | ||
| C. | K+ H+ HCO3- | D. | NH4+ Na+ OH- |
9.下列每组中两种物质反应时,无论哪种过量都可用同一离子方程式表示的是( )
| A. | FeBr2溶液与Cl2 | B. | Ca(HCO3)2溶液与KOH溶液 | ||
| C. | NaHCO3溶液与Al2(SO4)3溶液 | D. | NaHSO4溶液与Ba(OH)2溶液 |
10.某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀,该有机样品可能是( )
| A. | 乙酸 | B. | 乙醇 | ||
| C. | 乙醛 | D. | 甲醇和丙三醇的混合物 |
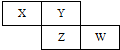 X、Y、Z、W四种短周期元素在周期表中的位置关系如图
X、Y、Z、W四种短周期元素在周期表中的位置关系如图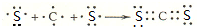 .
.