题目内容
 现有以下物质:①KCl晶体 ②食盐水 ③液态的醋酸 ④I2 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔融的NaOH⑨K2O ⑩SO2.请回答下列问题:
现有以下物质:①KCl晶体 ②食盐水 ③液态的醋酸 ④I2 ⑤BaSO4固体 ⑥蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔融的NaOH⑨K2O ⑩SO2.请回答下列问题:(1)以上物质中能导电的是
(2)以上物质属于电解质的是
(3)以上物质中属于非电解质的是
(4)从②溶液中得到氯化钠固体,应选择下列装置中的
(5)请写出③和⑧中两种物质的溶液混合后发生反应的离子方程式:
(6)在标准状况下,
考点:电解质与非电解质,物质的量的相关计算,物质的分离、提纯和除杂
专题:基本概念与基本理论
分析:(1)据物质导电的原因分析,只要含有自由移动的离子或自由电子即可;
(2)根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质;
(3)非电解质是在水溶液里或熔融状态下都不能导电的化合物,该定义的前提必须是化合物;
(4)从溶液中得到氯化钠固体,需要通过蒸发操作完成;分离碘单质和酒精,需要通过蒸馏操作完成;
(5)醋酸与氢氧化钾反应生成醋酸钾和水,醋酸在离子方程式中需要保留分子式;
(6)34.2g蔗糖的物质的量为0.1mol,含有1.1mol氧原子,据此计算出需要二氧化硫的物质的量及标况下的体积.
(2)根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质;
(3)非电解质是在水溶液里或熔融状态下都不能导电的化合物,该定义的前提必须是化合物;
(4)从溶液中得到氯化钠固体,需要通过蒸发操作完成;分离碘单质和酒精,需要通过蒸馏操作完成;
(5)醋酸与氢氧化钾反应生成醋酸钾和水,醋酸在离子方程式中需要保留分子式;
(6)34.2g蔗糖的物质的量为0.1mol,含有1.1mol氧原子,据此计算出需要二氧化硫的物质的量及标况下的体积.
解答:
解:(1)②食盐水中有钠离子和氯离子,所以能导电,满足条件的有:⑧熔融的NaOH中有自由移动的离子,所以能导电,
故答案为:②⑧;
(2)在水溶液里或熔融状态下能导电的化合物是电解质,所以满足条件的有:①KCl晶体、③液态的醋酸、⑤BaSO4固体、⑧熔融的NaOH⑨K2O 是电解质,
故答案为:①③⑤⑧⑨;
(3)非电解质是在水溶液里或熔融状态下都不能导电的化合物,满足条件的为:⑥蔗糖(C12H22O11)、⑦酒精(C2H5OH)、⑩SO2,
故答案为:⑥⑦⑩;
(4)从②氯化钠溶液中得到氯化钠固体,需要通过蒸发操作完成,所以应选择下列装置中的A;分离④碘单质与⑦酒精的混合液,需要通过蒸馏操作完成,所以应选择下列装置中的D,
故答案为:A; D;
(5)氢氧化钾与醋酸反应的离子方程式为:CH3COOH+OH-=CH3COO-+H20,
故答案为:CH3COOH+OH-=CH3COO-+H20;
(6)34.2g蔗糖的物质的量为0.1mol,0.1mol蔗糖中含有1.1molO原子,需要二氧化硫的物质的量为0.55mol,需要标况下二氧化硫的体积为:22.4L/mol×0.55mol=12.32L,
故答案为:12.32.
故答案为:②⑧;
(2)在水溶液里或熔融状态下能导电的化合物是电解质,所以满足条件的有:①KCl晶体、③液态的醋酸、⑤BaSO4固体、⑧熔融的NaOH⑨K2O 是电解质,
故答案为:①③⑤⑧⑨;
(3)非电解质是在水溶液里或熔融状态下都不能导电的化合物,满足条件的为:⑥蔗糖(C12H22O11)、⑦酒精(C2H5OH)、⑩SO2,
故答案为:⑥⑦⑩;
(4)从②氯化钠溶液中得到氯化钠固体,需要通过蒸发操作完成,所以应选择下列装置中的A;分离④碘单质与⑦酒精的混合液,需要通过蒸馏操作完成,所以应选择下列装置中的D,
故答案为:A; D;
(5)氢氧化钾与醋酸反应的离子方程式为:CH3COOH+OH-=CH3COO-+H20,
故答案为:CH3COOH+OH-=CH3COO-+H20;
(6)34.2g蔗糖的物质的量为0.1mol,0.1mol蔗糖中含有1.1molO原子,需要二氧化硫的物质的量为0.55mol,需要标况下二氧化硫的体积为:22.4L/mol×0.55mol=12.32L,
故答案为:12.32.
点评:本题考查了电解质溶液导电的原因及电解质、非电解质的定义,能导电的不一定是电解质,如硝酸钾溶液;电解质不一定能导电,如硫酸铜晶体.

练习册系列答案
相关题目
在含有大量K+、OH-、CO32-的溶液中还可能大量存在的离子是( )
| A、NH4+ |
| B、Al3+ |
| C、Ca2+ |
| D、SO42- |


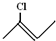 表示的分子式
表示的分子式 的键线式的表达式
的键线式的表达式 有的官能团的名称分别为
有的官能团的名称分别为
