题目内容
下列叙述正确的是
A.将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3
B.对于可逆反应N2(g)+3H2(g) 2NH3(g)增大氮气浓度可增加活化分子百分数,从而使反应速率增加
2NH3(g)增大氮气浓度可增加活化分子百分数,从而使反应速率增加
C.室温下,向Mg(OH)2中加入饱和氯化铵溶液能使Mg(OH)2溶解
D.恒容密闭容器中进行的反应3A(g) B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将减小
B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将减小
C
【解析】
试题分析:AlCl3溶液蒸干后可以完全水解得到Al(OH)3,灼烧得到Al2O3,但NaAlO2溶液蒸干不会完全水解,所得固体物为NaAlO2,A错;增大氮气浓度是增加活化分子数,而不是增加活化分子百分数,B错;Mg(OH)2 +2NH4Cl =Mg Cl2 + NH3·H2O,Mg(OH)2溶解,C对;充入A气体,相当于增大压强,平衡向正向移动,转化率增大,D错。
考点:盐类水解、有效碰撞理论和化学平衡移动。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
 2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的
2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的 )
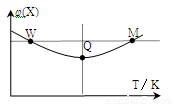
) 3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。
3Z(g)△H<0反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。