题目内容
18.2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖,由青蒿素合成衍生药物蒿甲醚的合成线路如下:下列说法正确的是( )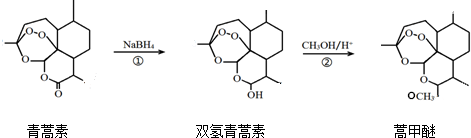
| A. | ①、②反应依次为加成反应、取代反应 | |
| B. | 上述三种有机物的含氧官能团完全相同 | |
| C. | 青蒿素因含酯基具有氧化性和杀菌功能 | |
| D. | 蒿甲醚的化学式为C16H24O5 |
分析 A.①中C=O转化为-OH,②中-OH上H被甲基取代;
B.青蒿素含-COOC-,而另两种有机物不含;
C.青蒿素中含有-O-O-化学键,与双氧水分子结构(H-O-O-H)相似;
D.由结构可知分子式.
解答 解:A.①中C=O转化为-OH,②中-OH上H被甲基取代,则分别发生加成、取代反应,故A正确;
B.青蒿素含-COOC-,而另两种有机物不含,则三种有机物中的官能团不完全相同,故B错误;
C.青蒿素中含有-O-O-化学键,与双氧水分子结构(H-O-O-H)相似,则具有强氧化性,可杀菌消毒,但与酯基无关,故C错误;
D.由蒿甲醚结构可知分子式为C16H26O5,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与迁移应用能力的考查,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
相关题目
8.现拟分离乙酸乙酯、乙酸、乙醇的混合物,图是分离操作流程图.
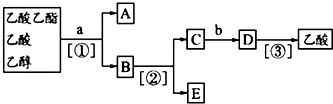
上述实验过程中涉及的三次分离操作分别是( )

上述实验过程中涉及的三次分离操作分别是( )
| A. | ①蒸馏 ②过滤 ③分液 | B. | ①分液 ②蒸馏 ③蒸馏 | ||
| C. | ①蒸馏 ②分液 ③分液 | D. | ①分液 ②蒸馏 ③结晶 过滤 |
9.工业碳酸钠(纯度约为98%)中常含有Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等杂质.为了提纯工业碳酸钠,并获得试剂级碳酸钠,采取工艺流程如图所示:
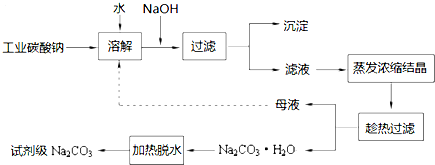
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
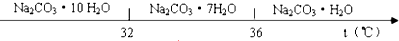
Ⅱ.有关物质的溶度积如下
(1)加入NaOH溶液主要为了除去Mg2+(填离子符号),发生反应的离子方程式为MgCO3+2OH-=Mg(OH)2+CO32-、Mg2++2OH-=Mg(OH)2↓;“沉淀”的主要成份有Mg(OH)2、Fe(OH)3、CaCO3(填化学式);
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021.
(2)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)Na2CO3在溶液中存在水解平衡CO32-+H2O?HCO3-+OH-,溶液呈碱性,当温度升高时水解平衡正向移动,使溶液碱性增强,故去油污能力增强.
(3)“趁热过滤”时的温度应控制在高于36℃.
(4)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73KJ/mol.
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用.请你分析实际生产中是否可行不可行,其理由是若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质.

已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
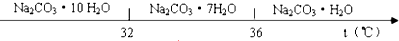
Ⅱ.有关物质的溶度积如下
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021.
(2)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)Na2CO3在溶液中存在水解平衡CO32-+H2O?HCO3-+OH-,溶液呈碱性,当温度升高时水解平衡正向移动,使溶液碱性增强,故去油污能力增强.
(3)“趁热过滤”时的温度应控制在高于36℃.
(4)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g)△H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式Na2CO3•H2O(s)=Na2CO3(s)+H2O(g)△H=+58.73KJ/mol.
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用.请你分析实际生产中是否可行不可行,其理由是若“母液”循环使用,则溶液c(Cl-)和c(SO42-)增大,最后所得产物Na2CO3中混有杂质.
6.下列说法正确的是( )
| A. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 | |
| B. | HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 | |
| C. | 元素周期律是元素原子核外电子排布周期性变化的结果 | |
| D. | 形成离子键的阴、阳离子间只存在静电吸引力 |
3.不法分子将毒品伪装成咖啡、麦片、面膜等贩卖到世界各地,已知部分毒品的结构简式如图,下列对毒品分类正确的是( )
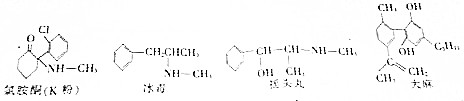

| A. | 盐 | B. | 氧化物 | C. | 有机物 | D. | 油脂 |
10.化学与生产、生活、环境等密切相关,下列关于消毒的说法正确的是( )
| A. | 医用酒精消毒的原理是将病毒氧化达到消毒目的 | |
| B. | 加热消毒是因为高温下蛋白质发生了变性 | |
| C. | 自来水净化过程中加入明矾的作用是消毒杀菌 | |
| D. | 使用84消毒液(有效成分次氯酸钠)时通入CO2或SO2均可增强消毒效果 |
2.下列烷烃分子中去掉一个氢原子后所得的烃基的结构最多的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烷 |