题目内容
一真空定容的密闭容器中盛有1mol PCl5,发生反应PCl5(g)?PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入2mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是( )
| A、M>N | B、M=N |
| C、M<N | D、无法比较 |
考点:化学平衡的计算
专题:
分析:加入2molPCl5所到达的平衡,可以等效为先将体积增大1倍到达的平衡状态,该状态与开始加入1molPCl5是完全相同的平衡状态,然后在将体积压缩恢复到原来的体积,增大压强后化学平衡向气体的体积减小的方向移动,据此进行判断PCl5的体积百分数的变化.
解答:
解:把加入2molPCl5所到达的平衡,可等效为先将容器体积增大1倍到达的平衡状态,该状态与开始加入1molPCl5是完全相同的平衡状态,然后在将体积压缩恢复到原来的体积,
增大压强后平衡向体积减小的方向移动,即平衡向逆反应方向移动,
所以PCl5的分解率减小,PCl5所占的体积百分数最大,即:M<N,
故选C.
增大压强后平衡向体积减小的方向移动,即平衡向逆反应方向移动,
所以PCl5的分解率减小,PCl5所占的体积百分数最大,即:M<N,
故选C.
点评:本题考查了压强对化学平衡的影响,题目难度中等,注意掌握影响化学平衡的元素,正确运用等效平衡是解本题的关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
关于中和热测定的说法错误的是( )
| A、实验需用到的主要玻璃仪器包括大、小烧杯,温度计,环形玻璃搅拌棒及泡沫塑料板、碎泡沫塑料(或硬纸板、碎纸条)等 |
| B、盐酸与某强碱中和放出的热量随反应物用量的改变而改变,但中和热不变 |
| C、NaOH稍过量的目的是保证盐酸完全被NaOH中和 |
| D、测定结果准确与否的关键是尽量减小热量损失及准确读取混合溶液的最高温度等 |
下列说法正确的是( )
| A、金属钠应保存在水里以隔绝空气 |
| B、常温下铁能与水蒸气反应生成氢氧化铁和氢气 |
| C、可以用铁制品或铝制品容器盛冷的浓H2SO4 |
| D、铝较活泼,所以铝制品在空气中不能稳定存在 |
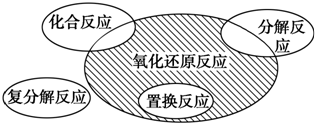
氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于阴影部分的是( )

A、Fe2O3+3CO
| ||||
B、2KClO3
| ||||
C、Na2O2+2Na
| ||||
| D、Cl2+2KBr═Br2+2KCl |
按照HCl、( )、Ca(ClO)2、KClO3、HClO4的排列规律,括号内应填入物质是( )
| A、Cl2 |
| B、NaClO |
| C、NaClO2 |
| D、ClO2 |