题目内容
G是一种合成橡胶和树脂的重要原料;A是一种五元环状化合物,其分子中只有一种化学环境的氢原子;F有三种不同化学环境的氢原子,且原子个数比为2:2:3.已知:(其中R是烃基).
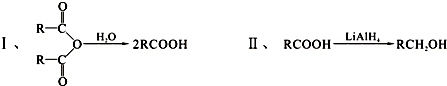
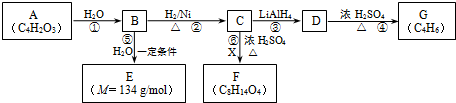
有关物质的转化关系如下图所示,请回答以下问题.
(1)C中所含官能团的名称是 ;②和④的反应类型分别是 反应、 反应.
(2)G的结构简式是 .
(3)若E在一定条件下发生缩聚反应生成聚酯类高分子化合物,写出其中两种的结构简式: 、 .
(4)反应⑥的化学方程式为 .
(5)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式: .
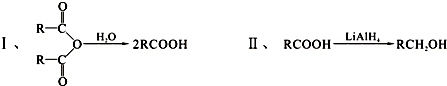
有关物质的转化关系如下图所示,请回答以下问题.

(1)C中所含官能团的名称是
(2)G的结构简式是
(3)若E在一定条件下发生缩聚反应生成聚酯类高分子化合物,写出其中两种的结构简式:
(4)反应⑥的化学方程式为
(5)有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,写出所有符合条件的Y的结构简式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A是一种五元环状化合物,其核磁共振氢谱只有一个峰,说明A中只含一种类型的H原子,A能水解生成B,B能和氢气发生加成反应生成C,说明B中含有碳碳双键,结合题给信息和A的分子式知,A的结构简式为: ,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,据此解答.
,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,据此解答.
 ,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,据此解答.
,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,据此解答.解答:
解:A是一种五元环状化合物,其核磁共振氢谱只有一个峰,说明A中只含一种类型的H原子,A能水解生成B,B能和氢气发生加成反应生成C,说明B中含有碳碳双键,结合题给信息和A的分子式知,A的结构简式为: ,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,
,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,
(1)C为HOOCCH2CH2COOH,所含官能团为羧基;反应②属于加成反应,反应④属于消去反应,故答案为:羧基;加成;消去;
(2)由上述分析可知,G的结构简式为:CH2=CHCH=CH2,故答案为:CH2=CHCH=CH2;
(3)若E[HOOCCH2CH(OH)COOH]在一定条件下发生缩聚反应生成聚酯类高分子化合物,其中两种的结构简式为: 、
、 ,故答案为:
,故答案为: 、
、 ;
;
(4)反应⑥的化学方程式为:HOOCCH2CH2COOH+2CH3CH2OH
CH3CH2OOCCH2CH2COOCH2CH3+2H2O,故答案为:HOOCCH2CH2COOH+2CH3CH2OH
CH3CH2OOCCH2CH2COOCH2CH3+2H2O;
(5)有机物Y与E[HOOCCH2CH(OH)COOH]互为同分异构体,且具有相同的官能团种类和数目,所有符合条件的Y的结构简式有:HOOCCH(CH2OH)COOH HOOCC(OH)(CH3)COOH,
故答案为:HOOCCH(CH2OH)COOH HOOCC(OH)(CH3)COOH.
 ,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,
,A水解生成B,B的结构简式为HOOCCH=CHCOOH,B和氢气发生加成反应生成C,C的结构简式为HOOCCH2CH2COOH,B和水发生反应生成E,根据B和E的摩尔质量知,B发生加成反应生成E,所以E的结构简式为:HOOCCH2CH(OH)COOH,C和X反应生成F,根据F的分子式知,X是乙醇,F的结构简式为CH3CH2OOCCH2CH2COOCH2CH3,C反应生成D,结合题给信息知,D的结构简式为HOCH2CH2CH2CH2OH,D在浓硫酸、加热条件下反应生成G,根据G的分子式知,D发生消去反应生成G,G的结构简式为:CH2=CHCH=CH2,(1)C为HOOCCH2CH2COOH,所含官能团为羧基;反应②属于加成反应,反应④属于消去反应,故答案为:羧基;加成;消去;
(2)由上述分析可知,G的结构简式为:CH2=CHCH=CH2,故答案为:CH2=CHCH=CH2;
(3)若E[HOOCCH2CH(OH)COOH]在一定条件下发生缩聚反应生成聚酯类高分子化合物,其中两种的结构简式为:
 、
、 ,故答案为:
,故答案为: 、
、 ;
;(4)反应⑥的化学方程式为:HOOCCH2CH2COOH+2CH3CH2OH
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
(5)有机物Y与E[HOOCCH2CH(OH)COOH]互为同分异构体,且具有相同的官能团种类和数目,所有符合条件的Y的结构简式有:HOOCCH(CH2OH)COOH HOOCC(OH)(CH3)COOH,
故答案为:HOOCCH(CH2OH)COOH HOOCC(OH)(CH3)COOH.
点评:本题考查有机物推断,需要学生结合反应条件综合分析进行推断,侧重考查学生综合运用能力,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
相关题目
下列有关电解质溶液的说法正确的是( )
| A、在蒸馏水中滴加浓H2SO4,KW不变 |
| B、CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C、25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸>VNaOH |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
区分羊毛织品和尼龙布最简单的方法是( )
| A、灼烧并闻气味 |
| B、观察外观 |
| C、放在水中比较柔软性 |
| D、手摸,凭手感区分 |