题目内容
在25℃时,有pH=a(a≤6)的盐酸VaL和pH=b(b≥8)的NaOH溶液VbL.二者混合恰好完全中和.问:
(1)若a+b=14时,则
= (填数值);
(2)若a+b=13时,则
= (填数值);
(3)若a+b>14时,则
= (填表达式),且Va Vb(填“>”“<”或“=”).
(1)若a+b=14时,则
| Va |
| Vb |
(2)若a+b=13时,则
| Va |
| Vb |
(3)若a+b>14时,则
| Va |
| Vb |
考点:酸碱混合时的定性判断及有关ph的计算
专题:
分析:25℃时、有pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸与该NaOH溶液中和,需VbLNaOH溶液,则有VaL×10-amol/L=VbL×10b-14mol/L,整理可得:Va:Vb=10a+b-14,以此对各小题进行解答.
解答:
解:25℃时、pH为a的HCl溶液和pH为b的NaOH溶液,取VaL该盐酸用该NaOH溶液中和,需VbLNaOH溶液,则有VaL×10-amol/L=VbL×10b-14mol/L,即Va:Vb=10a+b-14,
(1)若a+b=14,则+a+b-14=0,所以
=10a+b-14=1,故答案为:1;
(2)若a+b=13,则:a+b-14=-1,所以
=10a+b-14=1:10=0.1,故答案为:0.1;
(3)若a+b>14,则:a+b-14>0,
=10a+b-14>1,即Va>Vb,故答案为:10a+b-14;>.
(1)若a+b=14,则+a+b-14=0,所以
| Va |
| Vb |
(2)若a+b=13,则:a+b-14=-1,所以
| Va |
| Vb |
(3)若a+b>14,则:a+b-14>0,
| Va |
| Vb |
点评:本题考查酸碱中和的计算,题目难度中等,明确酸碱中和时氢离子与氢氧根离子的物质的关系为解答本题的关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法.

练习册系列答案
相关题目
区分羊毛织品和尼龙布最简单的方法是( )
| A、灼烧并闻气味 |
| B、观察外观 |
| C、放在水中比较柔软性 |
| D、手摸,凭手感区分 |
一真空定容的密闭容器中盛有1mol PCl5,发生反应PCl5(g)?PCl3(g)+Cl2(g),一定条件下平衡时PCl5所占的体积百分数为M,若相同条件相同容器中,最初放入2mol PCl5,则平衡时,PCl5的体积百分数为N,下列结论正确的是( )
| A、M>N | B、M=N |
| C、M<N | D、无法比较 |
从对人体有害的角度考虑,你认为炒锅用下列哪种材料最好( )
| A、铝 | B、铁 | C、铜 | D、铝合金 |
在水溶液中能大量共存的一组离子是( )
| A、NH4+、Na+、Cl-、SO42- |
| B、K+、Mg2+、OH-、NO3- |
| C、H+、Ca2+、SiO32-、NO3- |
| D、K+、Al3+、ClO-、HCO3- |
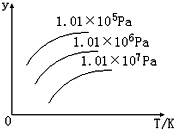 如图表示温度、压强对下列平衡的影响:N2 (g)+3H2(g)?2NH3(g)△H<0图中y轴表示的意义是( )
如图表示温度、压强对下列平衡的影响:N2 (g)+3H2(g)?2NH3(g)△H<0图中y轴表示的意义是( )| A、正反应速率 |
| B、平衡混合气体中NH3的含量 |
| C、平衡混合气体中N2的物质的量 |
| D、H2的转化率 |