题目内容
11.下列烯烃中存在顺反异构体的是( )| A. | 丙烯 | B. | 1-丁烯 | C. | 2-甲基-2-戊烯 | D. | 2-己烯 |
分析 具有顺反异构体的有机物中C=C应连接不同的原子或原子团,以此解答该题.
解答 解:A.丙烯为CH3CH=CH2,其中C=C连接相同的H原子,不具有顺反异构,故A错误;
B.1-丁烯为CH3CH2CH=CH2,其中C=C连接相同的H原子,不具有顺反异构,故B错误;
C.2-甲基-2-戊烯CH3C(CH3)=CHCH2CH3,其中C=C连接相同的H原子,不具有顺反异构,故C错误;
D.2-己烯为CH3CH=CHCH2CH2CH3,其中C=C连接不同的H、-CH3、-CH2CH2CH3,具有顺反异构,故D正确.
故选D.
点评 本题考查有机物的同分异构体,为高频考点,侧重于学生的分析能力的考查,题目难度中等,注意把握顺反异构的结构要求.

练习册系列答案
相关题目
1.对于amolH2O和amolCO2的说法正确的是( )
| A. | 相同条件下体积一定相同 | B. | 氧原子个数一定相同 | ||
| C. | 分子个数一定相同 | D. | 质量比是22:9 |
16. 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )
 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示.已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N放出942kJ热量,根据以上信息和数据,判断下列说法正确的是( )| A. | N4属于一种新型的化合物 | |
| B. | N4是N2的同素异形体 | |
| C. | N4分子中N-N键角为109°28′ | |
| D. | 1 mol N4转变成N2将吸收882 kJ热量 |
18.形成 1mol H-Cl键时放出431kJ的能量,断裂1molCl-Cl键时吸收243kJ的能量,断裂1mol H-H键时吸收436kJ的能量,则1mol H2(g)与1mol Cl2(g)完全反应生成2mol HCl(g)的能量变化为( )
| A. | 放出248 kJ的热量 | B. | 吸收248 kJ的热量 | ||
| C. | 放出183 kJ的热量 | D. | 吸收183 kJ的热量 |

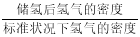 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为 。
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为 。