题目内容
12.若NA表示阿伏加德罗的数值,下列说法中正确的是( )| A. | 1molNa作为还原剂可得到的电子数为NA | |
| B. | 标准状况下,22.4L水中所含的水分子数为NA | |
| C. | 常温常压下,4g氦气含有的氦原子数为NA | |
| D. | 1mol Fe与足量的Cl2充分反应电子转移数为2NA |
分析 A.金属钠为1价金属,1mol钠失去1mol电子;
B.标况下,水为液态;
C.氦气是单原子分子;
D.铁被氯气氧化为氯化铁.
解答 解:A.1mol钠失去1mol电子,可得到的电子数为NA,故A正确;
B.标况下,水为液态,22.4L水的物质的量不是1mol,故B错误;
C.氦气是单原子分子,4g氦气的物质的量是1mol,故1mol氦气含1mol氦原子,个数为NA个,故C正确;
D.铁被氯气氧化为氯化铁,1mol Fe与足量的Cl2充分反应电子转移数为3NA,故D错误.
故选AC.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积是使用条件,明确方程式中电子转移的个数与量的关系是解题的关键.

练习册系列答案
相关题目
2.用1L0.5mol•L-1NaOH溶液吸收0.4molCO2,所以溶液中的CO32-和HCO3-的物质的量浓度之比约是( )
| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:1 |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L HF中含有原子数为2NA | |
| B. | 7.8 g Na2 0z中阴离子数目为0.2NA | |
| C. | 1 L 1 mol.L-1 KNO3溶液中O原子数为3NA | |
| D. | 常温常压下,44 g CO2和N2O的混合物中含有的质子数为22NA |
20.在催化剂作用下,H2O2发生分解,其反应能量随反应的进程变化如图,下列说法正确的是( )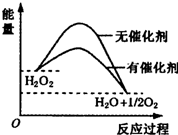

| A. | H2O2分解反应的△H>0 | |
| B. | 催化剂的加入使反应的热效应减小 | |
| C. | 催化剂的加入提高了H2O2的分解率 | |
| D. | 催化剂通过改变反应历程、降低反应的活化能来提高H2O2分解速率 |
17.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 0.1mol•L-1的氨水含有0.1NA个OH- | |
| B. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| C. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
4.常温时,下列块状金属中能全部溶于足量浓硝酸的是( )
| A. | Al | B. | Ag | C. | Fe | D. | Pt |
1.对下列物质进行的分类正确的是( )
| A. | 纯碱、烧碱均属于碱 | |
| B. | CuSO4•5H2O、液氨均属于纯净物 | |
| C. | 凡能电离出H+的化合物均属于酸 | |
| D. | NaCl H2SO4 BaSO4 NH3均属于电解质 |
2.下列物质属于电解质并能导电的是( )
| A. | 酒精 | B. | 氯化钾晶体 | ||
| C. | 液态氯化氢 | D. | 熔融态的氢氧化钠 |