题目内容
16.下列各组混合物能用分液漏斗分离的是( )| A. | 乙酸和乙醇 | B. | 乙酸乙酯和碳酸钠溶液 | ||
| C. | 溴苯和苯 | D. | 汽油和煤油 |
分析 能用分液漏斗分离的物质必须是两种相互不溶的液体,一般来讲:有机溶质易溶于有机溶剂,无机溶质易溶于无机溶溶剂,以此解答该题.
解答 解:题中乙醇和乙酸、溴苯和苯以及汽油和煤油都混溶,溶液不分层,不能用分液的方法分离,而乙酸乙酯不溶于饱和碳酸钠溶液,溶液分层,可用分液的方法分离,
故选B.
点评 本题考查了物质的分离和提纯,为高频考点,侧重考查学生的分析能力,题目难度不大,注意分液漏斗能分离的物质必须是互不相溶的液体,把握好常见的相互溶解和互不相溶的液体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.已知2SO2(g)+O2(g)?2SO3(g)(正反应方向放热).若在500℃和催化剂的作用下,该反应在容积固定的密闭容器中进行,下列有关说法正确的是( )
| A. | 若降低温度,可以加快反应速率 | |
| B. | 增大O2浓度可以增大反应速率 | |
| C. | 随着反应的进行,正反应速率逐渐减小,最后变为0 | |
| D. | 达到化学平衡状态时,SO2和SO3的浓度一定相等 |
11.化学与生产、生活、社会密切相关.下列说法错误的是( )
| A. | 使用布袋购物、以步代车属于“低碳生活”方式 | |
| B. | 饮用水中矿物质的含量越高越有利于人体健康 | |
| C. | 绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染 | |
| D. | 采用光触媒技术可将汽车尾气中的NO和CO转化为无毒气体 |
1.如图表示某有机反应的过程,该反应的类型是( )


| A. | 取代反应 | B. | 加成反应 | C. | 氧化反应 | D. | 加聚反应 |
8.KMnO4具有强氧化性,在实验室和工业上常用作氧化剂.某化学兴趣小组采用标准的酸性KMnO4溶液测定可能发生变质的还原性物质Na2SO3固体中Na2SO3的含量.
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
求样品中Na2SO3的质量分数63%.
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
| 编号溶液 | 1 | 2 | 3 | 4 |
| KMnO4(mL) | 20.01 | 19.00 | 19.99 | 20.00 |
| Na2SO3(mL) | 25.00 | 25.00 | 25.00 | 25.00 |
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
5.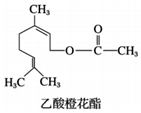 乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
①分子式为C12H19O2;
②不能发生银镜反应;
③1mol该有机物最多能与3mol氢气发生加成反应;
④它的同分异构体中不可能有酚类;
⑤1mol该有机物与NaOH溶液反应最多消耗1mol NaOH;
⑥属于芳香族化合物.
 乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )①分子式为C12H19O2;
②不能发生银镜反应;
③1mol该有机物最多能与3mol氢气发生加成反应;
④它的同分异构体中不可能有酚类;
⑤1mol该有机物与NaOH溶液反应最多消耗1mol NaOH;
⑥属于芳香族化合物.
| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑥ | D. | ②③④ |
4.下列判断错误的是( )
| A. | 稳定性:NH3>PH3>AsH3 | B. | 离子半径:Li+>O2->F- | ||
| C. | 酸性:H3PO4<H2SO4<HClO4 | D. | 碱性:LiOH<NaOH<KOH |

 碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题:
碳、镁、镍在工业生产和科研领域有广泛用途.请回答下列问题: )等.
)等. 是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.
是常用的分析试剂.其中位于同周期的三种基态原子第一电离能由小到大的顺序为C<O<N(用元素符号表示);这三种元素形成的一种离子与CS2互为等电子体,该离子符号为OCN-.