题目内容
18.设NA为阿伏加德罗常数的值,下列叙述错误的是( )| A. | 1.8g18O2分子与1.8g18O3分子中含有的中子数不同 | |
| B. | 7.8gNa2S和7.8g Na2O2中含有的阴离子数目均为0.1NA | |
| C. | 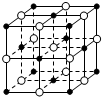 23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元 | |
| D. | 含16 g氧原子的二氧化硅晶体中含有的δ键数目为NA |
分析 A、18O2分子与18O3均由氧原子构成;
B、Na2S和 Na2O2的摩尔质量均为78g/mol,且均由2个钠离子和1个阴离子构成;
C、质量换算物质的量,结合一个晶胞含4个NaCl,计算分析;
D、求出二氧化硅的物质的量,然后根据1mol二氧化硅中含2molSi-O键来分析;
解答 解:A、18O2分子与18O3均由氧原子构成,故1.8g18O2分子与1.8g18O3中含有的18O的物质的量相同,均为0.1mol,则含有的中子数均为NA个,故A错误;
B、Na2S和 Na2O2的摩尔质量均为78g/mol,且均由2个钠离子和1个阴离子构成,故7.8gNa2S和 Na2O的物质的量均为0.1mol,其含有的阴离子均为0.1NA个,故B正确;
C、质量换算物质的量,结合一个晶胞含4个NaCl,23.4 g NaCl晶体物质的量=$\frac{23.4g}{58.5g/mol}$=0.4mol;所以含0.1 NA个如图所示结构单元,故C正确;
D、含16 g氧原子的二氧化硅的物质的量为$\frac{16g}{32g/mol}$=0.5mol,根据1mol二氧化硅中含2molSi-Oδ键可知,0.5mol二氧化硅晶体中含有的δ键数目为NA,故D正确;
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
20.在4P+3KOH+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$3KH2PO2+PH3↑的反应中,下列叙述正确的是( )
| A. | 磷仅被还原 | B. | 磷既被氧化又被还原 | ||
| C. | 有$\frac{3}{4}$的磷被还原 | D. | 有$\frac{1}{2}$的磷被氧化 |
1.物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质由浓度不同而能发生不同氧化还原反应的是( )
①Cu与HNO3溶液
②Cu与FeCl3溶液
③NH4Cl与NaOH溶液
④Fe与HCl溶液.
①Cu与HNO3溶液
②Cu与FeCl3溶液
③NH4Cl与NaOH溶液
④Fe与HCl溶液.
| A. | ① | B. | ①③ | C. | ①② | D. | ①③④ |
6.下列反应既属于离子反应,又属于氧化还原反应的是( )
| A. | Zn与稀硫酸的反应 | B. | 分解氯酸钾制氧气 | ||
| C. | NaOH溶液与盐酸中和 | D. | MgCl2溶液与KOH溶液产生沉淀 |
13.下列叙述中正确的是( )
| A. | 1 mol氢的质量是1 g | B. | 1 mol CO的质量为28 g•mol-1 | ||
| C. | 阿伏加德罗常数等于6.02×1023 | D. | 3.01×1023个SO2分子约是0.5 mol |
10.下列解释事实的方程式不正确的是( )
| A. | 明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| B. | 测0.1mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| C. | 水垢中的CaSO4用Na2CO3溶液处理:Ca2++CO32-=CaCO3↓ | |
| D. | NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-=SiO32-+H2O |
7.原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1.a-的电子层结构与氦相同,b
和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述正确的是( )
和c的次外层有8个电子,c-和d+的电子层结构相同.下列叙述正确的是( )
| A. | 元素的非金属性次序为c<b<a | |
| B. | a和其他3种元素均能形成共价化合物 | |
| C. | d和其他3种元素形成的化合物中的所有原子都达到8e-稳定结构 | |
| D. | 元素a、b、c各自最高和最低化合价的代数和分别为0、4、6 |
8.下列说法正确的是( )
| A. | 灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+ | |
| B. | 因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3═2NaIO3+Cl2不能发生 | |
| C. | 反应3NO2+H2O═2HNO3+NO中氧化剂和还原剂的物质的量之比是3:1 | |
| D. | 在反应CaH2+2H2O═Ca(OH)2+2H2↑中,水作氧化剂 |