题目内容
6.8.4gN2与9.6gR元素的某单质,所含原子个数相同,且分子数之比为3:2,则R的摩尔质量是48g/mol,该单质为O3.分析 先根据分子数之比为3:2可知二者物质的量之比为3:2,则N2与R相对分子质量之比$\frac{8.3}{3}$:$\frac{9.6}{2}$=7:12,利用N2相对分子质量求出R相对分子质量,从而可知其摩尔质量;再根据分子数目、分子组成与原子数目之间的关系求出含有原子数和R的相对原子质量,从而可判断R组成.
解答 解:分子数之比为3:2,所以N2与R相对分子质量之比$\frac{8.3}{3}$:$\frac{9.6}{2}$=7:12,
而N2相对分子质量为28,所以R相对分子质量=28×$\frac{12}{7}$=48,则其摩尔质量为48g/mol;
设R分子中含有原子数为x,由于两者所含原子个数相同,则:3×2=2x,解得:x=3,
所以R的相对原子质量为:$\frac{48}{3}$=16,R为O元素,该单质为O3,
故答案为:48g/mol;O3.
点评 本题考查了物质的量的计算,题目难度不大,明确摩尔质量与相对分子质量之间的关系为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数之间的关系,试题有利于培养学生的化学计算能力.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
16.铝与铍的性质相似.下列关于铍的性质推断中,正确的是( )
| A. | 氯化铍的水溶液呈酸性 | B. | 氢氧化铍可溶于水 | ||
| C. | 铍只与酸反应不与碱反应 | D. | 氧化铍的化学式为Be2O3 |
17.下列各物质中,互为同系物的是( )
| A. | 实验式相同的有机物 | B. | 油酸与软脂酸 | ||
| C. | 式量是16、44、58的有机物 | D. | 乙二醇和丙二醇 |
14.某药物的结构简式为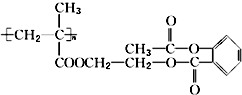 ,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
 ,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )| A. | 3 mol | B. | 4 mol | C. | 5 mol | D. | 4n mol |
1.下列叙述中错误的是( )
| A. | 稳定性:HF>HCl>HBr | B. | 还原性:Na>Mg>Al | ||
| C. | 原子半径:Cl>S>O | D. | 酸性:HClO4>H2SO4>H3PO4 |
11.将1molCO与1molCO2相比较.正确的是( )
| A. | 分子数为1:1 | B. | 原子数3:2 | C. | 电子数1:1 | D. | 质子数2:3 |
19.一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入( )
| A. | KCl固体 | B. | Zn粉 | C. | SO3固体 | D. | CuSO4晶体 |
20.下列说法错误的是( )
| A. | 氨气在一定条件下能和氧气反应 | |
| B. | 氨是一种易溶、易液化的气体 | |
| C. | 氨气能用浓硫酸来干燥 | |
| D. | 氨的水溶液能使红色石蕊试液变蓝色 |