题目内容
14.某药物的结构简式为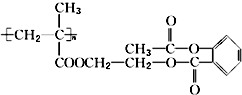 ,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
,1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为( )| A. | 3 mol | B. | 4 mol | C. | 5 mol | D. | 4n mol |
分析 由结构可知,分子中含-COOC-及水解生成的酚-OH均与NaOH反应,以此来解答.
解答 解:由结构可知,分子中含-COOC-为3n个,碱性条件下水解生成的酚-OH为n个,均与NaOH以1:1反应,则1mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为4nmol,
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意酯、酚的性质,题目难度不大.

练习册系列答案
相关题目
4.下列物质在一定条件下不能发生消去反应的是( )
| A. | (CH3)2CHCH2OH | B. | CH3CH2OH | C. | CH3CH2I | D. | CH3Cl |
5.发展绿色食品,避免“白色污染”,增强环保意识,是保护环境,提高人类生存质量的重要措施.“白色污染”是指( )
| A. | 白色建筑废料 | |
| B. | 聚乙烯等白色塑料垃圾 | |
| C. | 石灰窑的白色粉末 | |
| D. | 经济附加值高的营养食品和冶炼厂的白色烟尘 |
2.下列有关实验装置或实验操作正确的是( )
| A. | 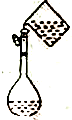 配置一定物质的量浓度的溶液 | B. | 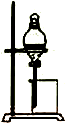 用CCl2萃取碘水中的溴 | ||
| C. | 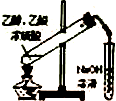 制备乙酸乙酯 | D. | 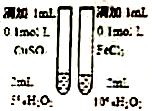 比较不同催化剂对反应速率的影响 |
9.下列方法或操作不能达到预期目的是( )
| 序号 | 实验目的 | 方法及操作 |
| ① | 比较水和乙醇中羟基氢的活泼性 强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 证明CH2=CHCHO中含有碳碳双 键 | 滴入KMn04酸性溶液,看紫红色是否褪去 |
| ③ | 证明蛋白质在某些无机盐溶液作 用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸铜溶液,有 沉淀析出;再把沉淀加入蒸馏水中 |
| ④ | 检验溴乙烷中的溴元素 | 将少量溴乙烷与NaOH溶液混合共热,充 分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgN03溶液 |
| A. | ① | B. | ② | C. | ③ | D. | ④ |
19.对于反应:N2+O2?2NO,在密闭容器中进行,下列条件中不能加快化学反应速率的是( )
| A. | 缩小体积使压强增大 | B. | 体积不变充入N2使气体压强增大 | ||
| C. | 体积不变充入Ne使气体压强增大 | D. | 升高温度 |
7.已知:相关物质的溶度积常数见表:
现有某酸性CuCl2溶液中含有少量的FeCl2,为得到纯净的CuCl2•2H2O晶体,按如图步骤进行提纯:

(1)最适合作氧化剂X的是C(填字母),加入X的目的是将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
加入的物质Y是CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3(填化学式),调至溶液pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反
应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.(I2+2S2O32-═S4O62-+2I-)
①可选用淀粉溶液作滴定指示剂.②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95%.
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

(1)最适合作氧化剂X的是C(填字母),加入X的目的是将Fe2+氧化成Fe3+,便于生成沉淀与Cu2+分离.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
加入的物质Y是CuO、Cu(OH)2、CuCO3、Cu2(OH)2CO3(填化学式),调至溶液pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=2.6×10-9mol/L.过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2•2H2O晶体.
(2)某学习小组用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I-发生反
应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.1000mol•L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.(I2+2S2O32-═S4O62-+2I-)
①可选用淀粉溶液作滴定指示剂.②CuCl2溶液与KI反应的离子方程式为2Cu2++4I-=2CuI↓+I2.
③该试样中CuCl2•2H2O的质量百分数为95%.
8.当光束通过下列分散系时,能产生丁达尔效应的是( )
| A. | NaCl溶液 | B. | Fe(OH)3胶体 | C. | 浓硫酸 | D. | 泥浆 |