题目内容
9.已知实验室制取C12的反应为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,又已知Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,也能氧化浓盐酸生成C12;(1)写出PbO2与浓盐酸反应的化学方程式PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O,其中表现还原性的HCl与表现酸性的HCl的物质的量之比为1:1.
(2)PbO2不稳定,随温度升高按下列顺序逐步分解:PbO2→Pb2O3→Pb3O4→PbO.若加热分解后所得到的固体全部为Pb3O4,现将a molPbO2加热分解,则加热过程中放出O2$\frac{22.4a}{3}$L(标准状况下);
(3)已知PbSO4不溶于水,但可溶于醋酸铵溶液,反应方程式如下:PbSO4+2CH3COONH4═(CH3COO)2Pb+(NH4)2SO4.
①PbSO4与CH3COONH4能进行反应的原因是符合了复分解反应条件之一的生成了难电离物质或弱电解质,现将Na2S溶液与醋酸铅溶液混合有沉淀生成,则其反应的离子方程式应为(CH3COO)2 Pb+S2-=PbS↓+2CH3COO-.
②已知+2价Sn的化合物具有强还原性.等物质的量的PbO2和SnO的混合物溶于过量的稀硫酸中,溶液中存在的主要金属阳离子是D(填序号).
A.Pb2+ B.Pb4+ C.Sn2+ D.Sn4+.
分析 (1)由题意可知,PbO2与浓盐酸反应生成PbCl2、Cl2与H2O,发生还原反应的HCl生成氯气,表现酸性的HCl生成PbCl2;
(2)根据Pb原子守恒计算n(Pb3O4),根据氧原子守恒计算生成氧气物质的量,再根据V=nVm计算氧气体积;
(3)①硫酸铅在水溶液里存在溶解平衡,加入醋酸铵时,醋酸根离子和铅离子生成难电离物质或弱电解质醋酸铅,促进硫酸铅溶解,醋酸铅能和硫化钠发生复分解反应生成黑色的硫化铅沉淀;
②+2价Sn的化合物具有强还原性,而+4价的Pb具有氧化性,等物质的量的PbO2和SnO的混合物溶于过量的稀硫酸中则发生氧化还原反应,而还原得到Pb2+与硫酸根离子结合为不溶于水的PbSO4.
解答 解:(1)由题意可知,PbO2与浓盐酸反应生成PbCl2、Cl2与H2O,反应方程式为:PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O,发生还原反应的HCl生成氯气,表现酸性的HCl生成PbCl2,反应中表现还原性的HCl与表现酸性的HCl的物质的量之比为1:1,
故答案为:PbO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O;1:1;
(2)根据Pb原子守恒,n(Pb3O4)=$\frac{1}{3}$n(PbO2)=$\frac{a}{3}$mol,根据氧原子守恒,生成氧气物质的量=$\frac{amol×2-\frac{a}{3}mol×4}{2}$=$\frac{a}{3}$mol,标况下氧气体积为$\frac{a}{3}$mol×22.4L/mol=$\frac{22.4a}{3}$L,
故答案为:$\frac{22.4a}{3}$;
(3)①硫酸铅在水溶液里存在溶解平衡,加入醋酸铵时,醋酸根离子和铅离子生成的醋酸铅,属于难电离物质或弱电解质,促进硫酸铅溶解,所以硫酸铅能溶于醋酸铵溶液中;醋酸铅能和硫化钠发生复分解反应生成黑色的硫化铅沉淀,符合复分解反应的条件,离子反应方程式为(CH3COO)2 Pb+S2-=PbS↓+2CH3COO-,
故答案为:难电离物质或弱电解质;(CH3COO)2 Pb+S2-=PbS↓+2CH3COO-;
②因为+2价Sn的化合物具有强还原性,而+4价的Pb具有氧化性,所以等物质的量的PbO2和SnO的混合物溶于过量的稀硫酸中则发生氧化还原反应生成Pb2+和Sn4+,Pb2+与硫酸根离子结合为不溶于水的PbSO4,则溶液中存在的主要金属阳离子是Sn4+,
故答案为:D.
点评 本题考查氧化还原反应有关计算、沉淀溶解平衡与转化等,侧重考查学生分析计算能力,题目难度中等,注意把握电子守恒在氧化还原反应计算中的应用方法.

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题:(1)以天然气为原料制H2是合成氨的一条重要的路线.甲烷的部分氧化可得到合成氨的原料气H2,其反应式如下:
①CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g)△H1=-35.6kJ•mol-1
有研究认为甲烷部分氧化的机理为:
②CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=-890.3kJ•mol-1
③CH4(g)+CO2(g)═2CO(g)+2H2(g)△H3=247.3kJ•mol-1
请结合以上条件写出CH4和H2O(g)生成CO和H2的热化学反应方程式:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=250.3kJ•mol-1.
(2)恒温下,向一个2L的密闭容器中充入1molN2和2.6molH2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/(mol/L) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②能提高反应中N2的平衡转化率的是BCE.
A.增加N2的浓度B.增加H2的量C.移出部分NH3D.提高反应温度
E.减小容器的容积F.加入合适的催化剂
(3)如图表示合成NH3反应在某段时间t0→t6中反应速率与反应过程的曲线图,若t1时改变的条件是升高温度,则在下列到达化学平衡的时间段中,NH3的体积分数最小的一段时间是(填写下列序号,下同)D,化学平衡常数最大的一段时间是A.
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
t4时改变的条件是减小压强.
(4)甲烷燃料电池(电解质溶液为KOH溶液)有广泛的应用.
①负极上发生的电极反应式是CH4+10OH--8e-=CO32-+7H2O.
②放电后,装置中溶液的pH变小.(填写“变大”、“变小”或“不变”)
| A. | 悬浊液 | B. | 乳浊液 | C. | 胶体 | D. | 溶液 |
| A. | 高容量的储氢材料研究是推广应用氢氧燃料电池的关键问题之一 | |
| B. | 大力发展新型电动汽车,可以减少燃油汽车的尾气排放量 | |
| C. | 生活中常用的蚕丝、棉花、淀粉、油脂等都是由高分子组成的物质 | |
| D. | 塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地且难以降解 |
| A. | 铝土矿(Al2O3) | B. | 磁性氧化铁(FeO) | ||
| C. | 铁红(Fe2O3) | D. | 明矾[KAl(SO4)2•12H2O] |
 +2B(g)
+2B(g) xC(g)△H=﹣192kJ•mol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
xC(g)△H=﹣192kJ•mol﹣1,向M、N中都通入1mol A和2mol B的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
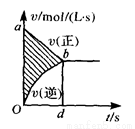
 2Z(g),并达到平衡。在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t关系如图。则图中阴影部分的面积可表示 (
2Z(g),并达到平衡。在此过程中,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间t关系如图。则图中阴影部分的面积可表示 (  )
)
 .X的浓度的减少 B.Y物质的量的减少
.X的浓度的减少 B.Y物质的量的减少