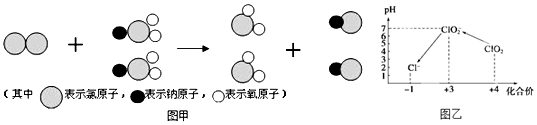
题目内容
1.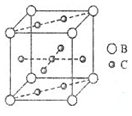 A、B、C、D、E、F六种元素,A、B、C属于第四周期元素且单质均为固体,原子处于基态时A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素,如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;E与F能形成原子数目比为1:3、熔点为190℃的化合物Q
A、B、C、D、E、F六种元素,A、B、C属于第四周期元素且单质均为固体,原子处于基态时A、B原子核外电子均成对,且核电荷数A>B;C与A在周期表属于同一区的元素,如图是金属B和C所形成的某种合金的晶胞结构示意图;D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的;E、F的原子均有三个能层,E原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;E与F能形成原子数目比为1:3、熔点为190℃的化合物Q(1)写出A的基态核外电子排布式1s22s22p63s23p63d104s2;用最简式表示B、C形成合金的组成CaCu5(用B、C元素符号表示).该合金的密度为 a g/cm3,其晶胞的边长为$\root{3}{\frac{360}{{N}_{A}a}}$cm.
(2)含有D、碳、硫三种元素的负一价离子中,所有原子均满足最外层8电子结构,一个电子是由硫原子所得,则其电子式为
 .
.(3)实验测得气态无水Q在1.Ol×105 Pa、t1℃的密度为5.OO g•L-1、气体摩尔体积为53.4L•mol-,则此时Q的组成为(写化学式)Al2Cl6,
(4)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似,则MgO 晶体中Mg2+的配位数是6,KCl、MgO、CaO 的熔点由高到低为MgO>CaO>KCl.
(5)紫外光的光子所具有的能量约为399kJ•mol-1.根据表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
分析 A、B、C、D、E、F六种元素,D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的,则D原子处于第二周期,外围电子排布为2s22p3,故D为氮元素;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:578,1817、2745、11575,E的最高价为+3,故E为铝元素;E与F能形成原子数目比为1:3,熔点为190℃的化合物,F为-1价,故F为氯元素,化合物Q熔点低,化合物Q是分子晶体;A、B、C属于第四周期且单质均为固体原子处于基态时,A、B原子核外电子均成对,A、B原子外围电子排布为4s2、3d104s2、4s24p6,且核电荷数A>B,故B为钙元素,A为锌元素;C与A在周期表属于同一区的元素,属于ds区,故C为铜元素.
解答 解:A、B、C、D、E、F六种元素,D、E、F均位于p区,D原子在基态时p轨道半充满且电负性是同族元素中最大的,则D原子处于第二周期,外围电子排布为2s22p3,故D为氮元素;E、F的原子均有三个能层,E原子的第一电离能至第四电离能(kJ/mol)分别为:578,1817、2745、11575,E的最高价为+3,故E为铝元素;E与F能形成原子数目比为1:3,熔点为190℃的化合物,F为-1价,故F为氯元素,化合物Q熔点低,化合物Q是分子晶体;A、B、C属于第四周期且单质均为固体原子处于基态时,A、B原子核外电子均成对,A、B原子外围电子排布为4s2、3d104s2、4s24p6,且核电荷数A>B,故B为钙元素,A为锌元素;C与A在周期表属于同一区的元素,属于ds区,故C为铜元素.
故A为锌元素、B为钙元素、C为铜元素、D为氮元素、E为铝元素、F为氯元素.
(1)A为锌元素,A的基态核外电子排布式为1s22s22p63s23p63d104s2;由晶胞结构可知,晶胞中Ca原子数目为8×$\frac{1}{8}$=1,Cu原子数目为1+8×$\frac{1}{2}$=5,B、C合金的组成为CaCu5;CaCu5的摩尔质量为360g/mol,设该晶胞的边长为x,根据密度公式:ρV=m,aNAx3=360,x=$\root{3}{\frac{360}{{N}_{A}a}}$cm;
故答案为:1s22s22p63s23p63d104s2;CaCu5;$\root{3}{\frac{360}{{N}_{A}a}}$cm;
(3)D为氮元素,碳、硫三种元素的负一价离子中,所有原子均满足最外层8电子结构,氮原子形成三键,碳原子形成4条共价键,硫原子形成2条共价键,其中一个电子是由硫原子所得,电子式为: ,
,
故答案为: ;
;
(4)实验测得气态无水Q在1.01ⅹ105Pa,t1℃的密度为5.00g/L,气体摩尔体积为53.4L/mol,该化合物的摩尔质量为5.00g/L×53.4L/mol=267g/mol,令化合物Q化学式为(AlCl3)n,所以:n×(27+35.5×3)=267,解得n=2,所以化合物Q化学式为Al2Cl6.
故答案为:Al2Cl6;
(5)KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似,TiN中离子都带3个单位电荷,MgO、CaO中离子都带2个单位电荷,KCl中离子都带1个单位电荷,离子半径Cl-<O2-<N3-,Mg2+<Ca2+<K+,高价化合物的晶格能远大于低价离子化合物的晶格,晶格能TiN>MgO>CaO>KCl,故熔点TiN>MgO>CaO>KCl;
在MgO晶胞中Mg2+周围有六个O2-,O2-周围有六个Mg2+,MgO 晶体中Mg2+的配位数是6,
故答案为:6;MgO>CaO>KCl;
(6)波长为300nm的紫外光的光子所具有的能量约为399kJ/mol,比蛋白质分子中C-C、C-N和C-S的键能都大,所以波长为300nm的紫外光的光子能破坏蛋白质分子中的化学键,从而破坏蛋白质分子.
故答案为:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
点评 本题考查核外电子排布规律、原子结构与物质关系、晶体结构与化学键等,题目难度中等,根据核外电子排布推断元素是关键,是对知识的综合考查.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,应立即用稀酸液冲洗 | |
| C. | 酒精灯着火时可用水扑灭 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
H2(g)+Cl2(g)═2HCl(g)△H2
2H2O(g)+2Cl2(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是( )
| A. | △H3═△H1+2△H2 | B. | △H3═△H1+△H2 | C. | △H3═△H1-2△H2 | D. | △H3═△H1-△H2 |
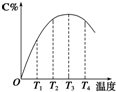 可逆反应A(g)+B(g)?2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示.
可逆反应A(g)+B(g)?2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示. 某同学用胆矾晶体(CuSO4•5H2O)配制0.05mol/L的CuSO4溶液980mL,回答下列问题:
某同学用胆矾晶体(CuSO4•5H2O)配制0.05mol/L的CuSO4溶液980mL,回答下列问题: