题目内容
下列有关实验的叙述中,正确的是( )
| A、容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 |
| B、用分液的方法分离水和酒精的混合物 |
| C、配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体 |
| D、用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁 |
考点:配制一定物质的量浓度的溶液,药品的取用,分液和萃取
专题:化学实验基本操作
分析:A、容量瓶中事先有水对所配溶液浓度无影响;
B、分液法用于分离互不相溶的液态混合物;
C、托盘天平能精确到0.1g;
D、滴加液体时,应垂直悬空.
B、分液法用于分离互不相溶的液态混合物;
C、托盘天平能精确到0.1g;
D、滴加液体时,应垂直悬空.
解答:
解:A、若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,故A正确;
B、分液法用于分离互不相溶的液态混合物,而水和酒精是混溶的,故不能用分液法来分离,故B错误;
C、托盘天平只能精确到0.1g,故C错误;
D、滴加液体时,应垂直悬空,故D错误.
故选A.
B、分液法用于分离互不相溶的液态混合物,而水和酒精是混溶的,故不能用分液法来分离,故B错误;
C、托盘天平只能精确到0.1g,故C错误;
D、滴加液体时,应垂直悬空,故D错误.
故选A.
点评:本题考查了配制一定物质的量浓度溶液时的仪器的使用和操作要点,难度不大,属于基础性题目.

练习册系列答案
相关题目
在120℃、101kPa下,a mL由氢气、乙烯组成的混合气体在b mL氧气中充分燃烧后,恢复到原温度和压强.已知b>3a,且燃烧后气体体积缩小了
mL,则乙烯的体积为( )
| b |
| 16 |
A、
| ||
B、
| ||
C、a-
| ||
D、
|
某兴趣小组为探究外界条件对可逆反应A(g)+B(g)═C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10L的密闭容器中充入1mol A和1mol B,反应达平衡时测得容器中各物质的浓度为Ⅰ.然后改变不同条件做了另三组实验,重新达到平衡时容器中各成分的浓度分别为Ⅱ、Ⅲ、Ⅳ.
针对上述系列实验,下列结论中错误的是( )
| A | B | C | |
| Ⅰ | 0.050mol?L-1 | 0.050mol?L-1 | 0.050mol?L-1 |
| Ⅱ | 0.070mol?L-1 | 0.070mol?L-1 | 0.098mol?L-1 |
| Ⅲ | 0.060mol?L-1 | 0.060mol?L-1 | 0.040mol?L-1 |
| Ⅳ | 0.080mol?L-1 | 0.080mol?L-1 | 0.12mol?L-1 |
| A、由Ⅰ中数据可计算出该温度下反应的平衡常数K=20mol-1?L |
| B、Ⅱ可能是通过增大C的浓度实现的 |
| C、若Ⅲ只是升高温度,则与Ⅰ比较,可以判断出正反应一定是放热反应 |
| D、第Ⅳ组实验数据的得出,只能通过压缩容器的体积才可以实现 |
下列说法正确的是( )
| A、CH4和Cl2以物质的量之比为1:1混合,光照下只生成CH3Cl和HCl |
| B、分子式为C3H5Cl3的同分异构体共有(不考虑立体异构)5种 |
C、 分子中所有原子可以处在同一平面上 分子中所有原子可以处在同一平面上 |
D、单体CH2═CHCH3和CH2═CH2可以通过加聚反应合成 |
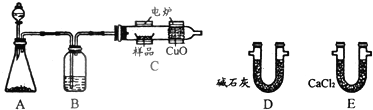
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
| A、①② | B、③④ | C、①③ | D、②④ |
下列说法不正确的是( )
| A、生铁、不锈钢和黄金都属于合金 |
| B、水泥、玻璃、陶瓷均属于无机非金属材料 |
| C、淀粉、油脂、蛋白质都属于天然高分子化合物 |
| D、天然气、石油液化气和汽油的主要成分都属于烃类 |
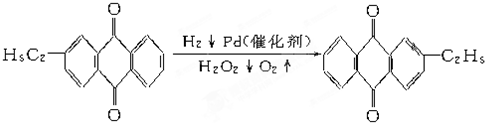
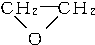 +CaCl2+H2O,则制备
+CaCl2+H2O,则制备 工艺的原子利用率为
工艺的原子利用率为