题目内容
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3→K2O+5Na2O+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
| A、生成42.0LN2(标准状况) |
| B、转移电子的物质的量为1.25mol |
| C、有0.250molKNO3被氧化 |
| D、被氧化的N原子的物质的量为1.875mol |
考点:氧化还原反应的计算,氧化还原反应
专题:氧化还原反应专题
分析:根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原,现氧化产物比还原产物多1.75mol,则生成2molN2,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,以此解答该题.
解答:
解:反应中NaN3中N元素化合价升高,被氧化,KNO3中N元素化合价降低,被还原,根据反应方程式可知,每当生成16molN2,则氧化产物比还原产物多14mol,转移电子的物质的量为10mol,被氧化的N原子的物质的量为30mol,有2molKNO3被还原,
现氧化产物比还原产物多1.75mol,则生成2molN2,在标准状况下的体积为44.8L,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,
故选B.
现氧化产物比还原产物多1.75mol,则生成2molN2,在标准状况下的体积为44.8L,转移电子的物质的量为1.25mol,被氧化的N原子的物质的量为3.75mol,
故选B.
点评:本题考查氧化还原反应知识,侧重于氧化还原反应的计算,注意根据化合价的变化结合方程式判断氧化产物和还原产物的物质的量关系为解答该题的关键,题目难度不大.

练习册系列答案
相关题目
可确认发生了化学平衡移动的是( )
| A、由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 |
| B、有气态物质参加的可逆反应达到平衡后,改变了压强 |
| C、化学反应速率发生了改变 |
| D、可逆反应达到平衡后,使用催化剂 |
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入( )
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
①饱和NaHCO3溶液;无水CaCl2固体
②饱和NaHCO3溶液;浓硫酸
③浓硫酸;饱和NaHCO3溶液
④饱和Na2CO3溶液;稀硫酸.
| A、①② | B、③④ | C、①③ | D、②④ |
以下是某学生的实验操作,正确的是( )
| A、用酒精萃取碘水中的碘 |
| B、用CCl4分离苯和溴苯 |
| C、用裂化汽油萃取溴水中的溴 |
| D、将金属钠保存于十二烷中 |
Mg和Al都是较活泼的金属,下列说法正确的是( )
A、Mg+2RbCl
| ||||
| B、在由镁铝形成的原电池中,负极反应一定是:Mg-2e-═Mg2+ | ||||
| C、MgCl2、AlCl3溶液分别加热蒸发、灼烧,均可得到氧化镁和氧化铝 | ||||
| D、因为氧化镁和氧化铝都是高熔点的物质,所以工业上分别用电解熔融MgCl2和AlCl3的方法制取镁和铝 |
化学与生活密切相关,下列说法正确的是( )
| A、二氧化硫广泛用于食品的漂白 |
| B、生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其单体的分子式为C8H10 |
| C、合成纤维,人造纤维及碳纤维都属于有机高分子材料 |
| D、先通入氯气,再加入硫酸亚铁处理水,能达到消毒杀菌和除去悬浮杂质的目的 |
如果用排水法收集浓硝酸受热分解所产生的气体,则( )
| A、收集到NO |
| B、收集到NO2 |
| C、收集到O2 |
| D、收集不到任何气体 |
有关实验操作,不能达到预期目的是( )
| A、用10mL量筒量取8.2mL水 |
| B、用电子天平称取5.6g氧化铜粉末 |
| C、用排水集气法可得到比较纯净的氧气 |
| D、用5mL水和5mL酒精配制成10mL酒精溶液 |
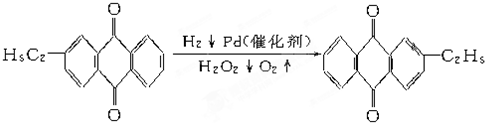
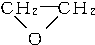 +CaCl2+H2O,则制备
+CaCl2+H2O,则制备 工艺的原子利用率为
工艺的原子利用率为