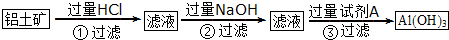题目内容
3.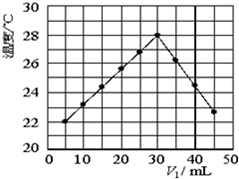 将V1mL1.0mol•L-1 H2SO4溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述不正确的是( )
将V1mL1.0mol•L-1 H2SO4溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述不正确的是( )| A. | 做该实验时环境温度可能为20℃ | B. | 该实验表明化学能可以转化为热能 | ||
| C. | NaOH溶液的浓度约是1.5mol•L-1 | D. | 该实验表明中和反应是放热反应 |
分析 A.实验时的温度应为酸碱未混合之前的温度;
B.反应时温度升高;
C.恰好反应时参加反应的H2SO4溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,以此计算NaOH浓度;
D.根据一个反应无法得出此结论.
解答 解:A.温度为22℃时加入盐酸10mL,中和反应放热,实验时环境温度要低于22℃,故A正确;
B.反应时温度升高,说明化学能转化为热能,故B正确;
C.恰好反应时参加反应的H2SO4溶液的体积是30mL,由V1+V2=50mL可知,消耗的氢氧化钠溶液的体积为20mL,恰好反应时氢氧化钠溶液中溶质的物质的量是n,由H2SO4+2NaOH=Na2SO4+2H2O可知,n=2×1.0mol•L-1×0.03L=0.06mol,所以浓度c=$\frac{0.06mol}{0.02L}$=3mol/L,故C错误;
D.该反应是中和反应,反应放热,不能表明中和反应是放热反应,所以D错误;
故选CD.
点评 本题考查中和反应、溶液pH的计算,题目难度中等,试题侧重学生图象及中和实质的考查,训练学生观察分析问题的能力,以及利用化学方程式计算的能力,比较综合.

练习册系列答案
相关题目
20.某气体MO2在20℃、1.013x105 Pa的条件下,对氢气的相对密度是23,则M的相对原子质量是( )
| A. | 12 | B. | 14 | C. | 28 | D. | 32 |
1.下列有关说法错误的是( )
| A. | 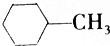 的一氯代物最多有4种 的一氯代物最多有4种 | |
| B. | 乙酸可与乙醇、金属钠、新制Cu(OH)2悬浊液等物质反应 | |
| C. | Cl2可与乙烷发生取代反应,与乙烯发生加成反应 | |
| D. | 阿托酸(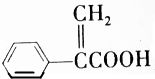 )可用于合成高分子材料 )可用于合成高分子材料 |
18.取一定量含FeO、Fe3O4和Fe2O3的固体混合物,将其分成两等份并进行下列转化:
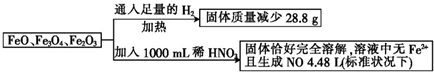
若稀HNO3恰好完全反应,则所加稀HNO3的物质的量浓度为( )

若稀HNO3恰好完全反应,则所加稀HNO3的物质的量浓度为( )
| A. | 4.0 mol•L-1 | B. | 4.4 mol•L-1 | C. | 4.8 mol•L-1 | D. | 3.6 mol•L-1 |
8.下列化学用语书写正确的是( )
| A. | 醋酸与NaOH溶液反应的离子方程式为:H++OH-═H2O | |
| B. | 金属钠与乙醇反应的化学方程式为:2Na+2CH3CH2OH→2CH3CH2ONa+H2↑ | |
| C. | 聚氯乙烯的结构简式为: | |
| D. | 氯化铵的电子式为: |
 .
.