题目内容
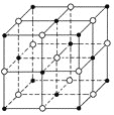
【题目】如图所示,食盐晶体由钠离子和氯离子构成。已知食盐的M=58.5g·mol-1,食盐的密度是2.2g·cm-3,阿伏加德罗常数为6.0×1023mol-1,在食盐晶体中两个距离最近的钠离子中心间的距离最接近下列哪个数据( )
A.3.0×10-8cmB.3.5×10-8cmC.4.0×10-8cmD.5.0×10-8cm
【答案】C
【解析】
根据晶胞结构图可知,每个晶胞中有钠离子8×![]() +6×
+6×![]() =4个,氯离子1+12×
=4个,氯离子1+12×![]() =4个,根据ρ=
=4个,根据ρ=![]() 可计算出晶胞的体积为
可计算出晶胞的体积为 cm3=1.77×10-22cm3,所以晶胞的边长为5.61×10-8cm,所以晶胞的碳对角线长为
cm3=1.77×10-22cm3,所以晶胞的边长为5.61×10-8cm,所以晶胞的碳对角线长为![]() ×5.61×10-8cm=8.0×10-8cm,在食盐晶体中两个距离最近的钠离子中心间的距离为晶胞面对角线的一半,所以两个距离最近的钠离子中心间的距离为4.0×10-8cm,故答案为C。
×5.61×10-8cm=8.0×10-8cm,在食盐晶体中两个距离最近的钠离子中心间的距离为晶胞面对角线的一半,所以两个距离最近的钠离子中心间的距离为4.0×10-8cm,故答案为C。

【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是:
A. 反应达到平衡时,X的转化率为50% B. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 C. 增大压强使平衡向生成Z的方向移动,平衡常数增大 D. 改变温度可以改变此反应的平衡常数
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
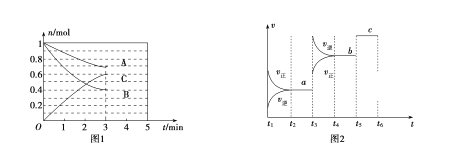
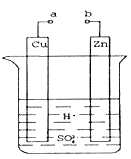
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。

①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
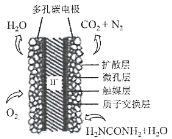
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。