题目内容
【题目】一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mo1)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
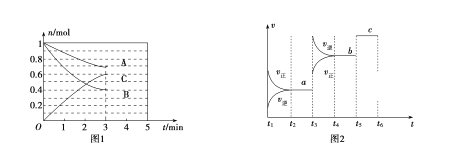
(1)该反应的化学方程式为__________________,此反应平衡常数的表达式为K=________。
(2)从开始到最初达到平衡,C的平均反应速率v(C)=________________。3min时,A的转化率=________%。该反应的![]() ________0。(填“
________0。(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”)
”)
(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡______移动(填“正向”、“逆向”或“不”,下同)
②恒温恒压充入惰性气体,平衡______移动,化学反应速率_______(填“加快”或“减慢”)
③升高温度,平衡______移动。
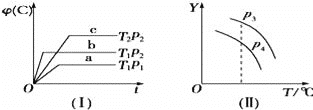
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是_______,t5时刻改变的外界条件是_______。
②a、b、c三个阶段中,C的体积分数最大的是________,
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3 之间的关系为___________(用“![]() ”、“
”、“![]() ”或“
”或“![]() ”连接)。
”连接)。
【答案】A(g)+2B(g)2C(g) 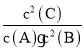 0.04mol·L-1·min-1 30 < 不 逆向 减慢 逆向 升高温度 加入催化剂 a K1>K2=K3
0.04mol·L-1·min-1 30 < 不 逆向 减慢 逆向 升高温度 加入催化剂 a K1>K2=K3
【解析】
(1)由图1中曲线变化情况可知:A和B是反应物,C是生成物,再由物质的量的变化值可得化学计量数之比;由图1可知,最后A、B的物质的量不为0,为可逆反应,3min时△n(A):△n(B):△n(C)=(1-0.7)mol:(1-0.4)mol:0.6mol=1:2:2,物质的量之比等于化学计量数之比,由此可以推出方程式;
(2)v(C)= ![]() =
=![]() ;降低温度,反应向放热方向移动,降低温度后A的体积分数减小,说明正反应是放热反应,则△H<0;
;降低温度,反应向放热方向移动,降低温度后A的体积分数减小,说明正反应是放热反应,则△H<0;
(3) ①恒温恒容充入惰性气体,各反应物反应速率不变,平衡不移动;
②恒温恒压充入惰性气体,各反应物浓度减小,反应速率减小,等效于减小压强,A(g)+2B(g)2C(g)是气体体积减小的反应,减小压强,平衡逆向移动;
③该反应△H<0,放热,升高温度,反应逆向移动;
(4)①t3时刻改变条件,正逆反应速率都增大,且平衡向逆反应方向进行,则改变的条件是升高温度;t5时刻正逆反应速率都增大,平衡不移动,则改变的条件是加入催化剂;
②a处是正反应速率大于逆反应速率后达到的平衡状态,平衡正向移动,C的体积分数增大;b、c均是逆反应速率大于正反应速率后达到的平衡状态,平衡逆向移动,C的体积分数减小,故C的体积分数最大的是a;
③该反应正反应是放热反应,所以升高温度平衡常数减小,因为t3升高温度,所以K1>K2,t5使用催化剂,所以K2=K3,该反应为放热反应所以K1>K2=K3。
(1)由图1中曲线变化情况可知:A和B是反应物,C是生成物,再由物质的量的变化值可得化学计量数之比;由图1可知,最后A、B的物质的量不为0,为可逆反应,3min时△n(A):△n(B):△n(C)=(1-0.7)mol:(1-0.4)mol:0.6mol=1:2:2,物质的量之比等于化学计量数之比,所以反应方程式为A(g)+2B(g)2C(g);平衡常数为生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,所以K= 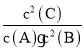 ;
;
(2)v(C)= ![]() =
=![]() =
= =0.04mol·L-1·min-1;A的转化率=
=0.04mol·L-1·min-1;A的转化率=![]() =30%;降低温度,反应向放热方向移动,降低温度后A的体积分数减小,说明正反应是放热反应,则△H<0;
=30%;降低温度,反应向放热方向移动,降低温度后A的体积分数减小,说明正反应是放热反应,则△H<0;
(3) ①恒温恒容充入惰性气体,各反应物反应速率不变,平衡不移动;
②恒温恒压充入惰性气体,各反应物浓度减小,反应速率减小,等效于减小压强,A(g)+2B(g)2C(g)是气体体积减小的反应,减小压强,平衡逆向移动;
③该反应△H<0,放热,升高温度,反应逆向移动;
(4)①t3时刻改变条件,正逆反应速率都增大,且平衡向逆反应方向进行,则改变的条件是升高温度;t5时刻正逆反应速率都增大,平衡不移动,则改变的条件是加入催化剂;
②a处是正反应速率大于逆反应速率后达到的平衡状态,平衡正向移动,C的体积分数增大;b、c均是逆反应速率大于正反应速率后达到的平衡状态,平衡逆向移动,C的体积分数减小,故C的体积分数最大的是a;
③该反应正反应是放热反应,所以升高温度平衡常数减小,因为t3升高温度,所以K1>K2,t5使用催化剂,所以K2=K3,该反应为放热反应所以K1>K2=K3。