题目内容
17.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )| A. | 先滴加BaCl2溶液再滴加HCl溶液,生成白色沉淀,原溶液中有SO42- | |
| B. | 滴加氯水和CCl4,振荡、静置,上层溶液显紫色,原溶液中有I- | |
| C. | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色,原溶液中有Na+ | |
| D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ |
分析 A.可能生成AgCl沉淀;
B.四氯化碳密度比水大;
C.钠的焰色反应为黄色;
D.氨气易溶于水.
解答 解:A.滴加氯化钡溶液,有白色沉淀生成,不能说明原溶液中有硫酸根离子,因为碳酸根离子、亚硫酸根离子、硫酸根离子、银离子等滴加氯化钡溶液,都成生成白色沉淀,故A错误;
B.氯水中的氯气和碘离子反应生成碘单质,四氯化碳把碘从水溶液中萃取出来,四氯化碳密度比水大,下层溶液显紫色,故B错误;
C.钠的焰色反应为黄色,可说明原溶液中有Na+,故C正确;
D.氨气极易溶于水,若溶液中含有少量的NH4+时,滴加稀NaOH溶液不会放出NH3,故D错误.
故选C.
点评 本题考查较为综合,涉及物质的制备、检验等基本实验操作,侧重于学生化学实验方案评价能力的考查,注意物质的检验要排除其它离子的干扰,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.如图是电解MgCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断不正确的是( )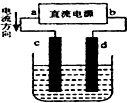

| A. | c、d电极上都有气体产生 | B. | d为阴极、c为阳极 | ||
| C. | d极附近溶液PH值升高 | D. | 电解过程中,氯离子浓度减小 |
12.下列说法正确的是( )
| A. | 任何情况下,温度都不可能对反应的方向起决定性作用 | |
| B. | pH=4的CH3COOH和NH4Cl溶液中,水的电离程度相同 | |
| C. | 用pH试纸测定溶液pH的正确操作是,将一小条试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照 | |
| D. | pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
2.下列过程需要通电才能进行的是( )
①电离 ②电镀 ③电解 ④电化学腐蚀.
①电离 ②电镀 ③电解 ④电化学腐蚀.
| A. | ①② | B. | ②③ | C. | ③④ | D. | 全部 |
9.如图甲是利用一种微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )
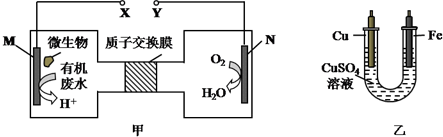

| A. | H十透过质子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25mol气体时,则铁电极增重16g |
6.银器的保护主要是维持它的原貌,对于轻微腐蚀蒙有硫化银的银器,可将其和铝片一起接触浸泡在稀NaOH溶液中,经一定时间污迹消失,取出后用水洗干净,再用软布或棉团擦光.有关叙述正确的是( )
| A. | 溶液中的OH-向正极移动 | |
| B. | 在银表面上的反应为:2Al+3Ag2S═6Ag+Al2S3 | |
| C. | 正极反应式为:Ag2S+2e-═2Ag+S2- | |
| D. | 在铝表面的反应为:Al+3OH--3e-═Al(OH)3 |
7.将0.06mol FeCl2加入100ml K2Cr2O7溶液中,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-被还原为Cr3+.则K2Cr2O7溶液的物质的量浓度为( )
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
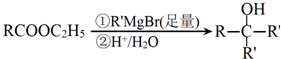
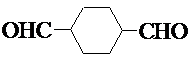 .
.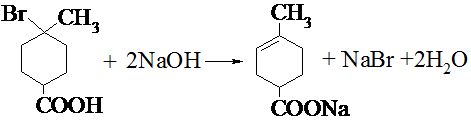 .
.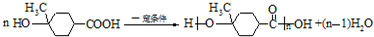 .
. .
.