题目内容
9.如图甲是利用一种微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )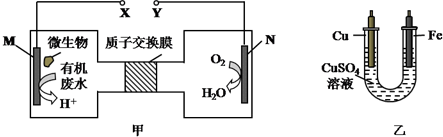
| A. | H十透过质子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.25mol气体时,则铁电极增重16g |
分析 根据题给信息知,该装置是将化学能转化为电能的原电池,由甲图可知,M是负极,N是正极,电解质溶液为酸性溶液,负极上失电子发生氧化反应,正极上得电子发生还原反应,在铁上镀铜,则铁为阴极应与负极相连,铜为阳极应与正极相连,根据得失电子守恒计算,以此解答该题.
解答 解:该装置是将化学能转化为电能的原电池,由甲图可知,M是负极,N是正极,电解质溶液为酸性溶液,负极上失电子发生氧化反应,正极上得电子发生还原反应,
A.M是负极,N是正极,质子透过离子交换膜由左M极移向右N极,故A错误;
B.铁上镀铜,则铁为阴极应与负极相连,铜为阳极应与正极Y相连,故B错误;
C.H2NCONH2在负极M上失电子发生氧化反应,生成但其、二氧化碳和水,电极反应式为H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+,故C正确;
D.当N电极消耗0.25mol氧气时,则转移0.25×4=1.0mol电子,所以铁电极增重$\frac{1}{2}$mol×64g/mol=32g,故D错误.
故选C.
点评 本题考查了原电池原理以及电镀原理,为高频考点,侧重于学生的分析、计算能力的考查,明确原电池正负极上得失电子、电解质溶液中阴阳离子移动方向即可解答,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.反应:aL(s)+bG(g)?cR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,
x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )
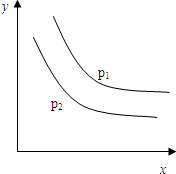
x轴表示温度,y轴表示平衡混合气中G的体积分数.据此可判断( )

| A. | 上述反应是放热反应 | B. | 上述反应是吸热反应 | ||
| C. | a+b>c | D. | a+b<c |
20.下列说法正确的是( )
| A. | 润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 | |
| B. | 用惰性电极电解MgCl2溶液的离子方程式为:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵溶液和稀酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 | |
| D. | 嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体 |
17.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| A. | 先滴加BaCl2溶液再滴加HCl溶液,生成白色沉淀,原溶液中有SO42- | |
| B. | 滴加氯水和CCl4,振荡、静置,上层溶液显紫色,原溶液中有I- | |
| C. | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色,原溶液中有Na+ | |
| D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ |
1.合金在现代生产、生活中应用非常广泛,因为它有许多优良的特性,下列关于合金性质的说法错误的是( )
| A. | 多数合金的硬度一般比其各成分金属的硬度高 | |
| B. | 多数合金的熔点一般比其各成分金属的熔点低 | |
| C. | 合金中可以含有非金属元素 | |
| D. | 合金的化学性质一般与其各成分金属的化学性质不同 |
18.下列说法正确的是( )
| A. | Mg、Al在空气中性质稳定,因而都具有很强的抗腐蚀性 | |
| B. | 质量数相等的不同核素,一定属于不同种元素 | |
| C. | 生石灰、铁粉、硅胶是食品包装中常用的干燥剂 | |
| D. | 自行车钢架生锈主要是化学腐蚀所致 |
19.下列离子方程式与所述事实相符且书写正确的是( )
| A. | 用铁作电极电解饱和氯化钠溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 肥皂水能使酚酞试液变红:C17H35COO-+H2O?C17H35COOH+OH- | |
| C. | FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2═2Fe3++2H2O | |
| D. | 已知苯甲酸的酸性比碳酸强,向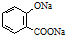 溶液中通入过量CO2: 溶液中通入过量CO2: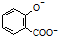 +2CO2+2H2O→ +2CO2+2H2O→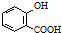 +2HCO3- +2HCO3- |

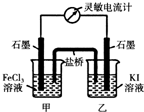 常温下,将FeCl3溶液和KI溶液混合,发生如下反应:2Fe3++2I-?2Fe2++I2
常温下,将FeCl3溶液和KI溶液混合,发生如下反应:2Fe3++2I-?2Fe2++I2