题目内容
2.下列过程需要通电才能进行的是( )①电离 ②电镀 ③电解 ④电化学腐蚀.
| A. | ①② | B. | ②③ | C. | ③④ | D. | 全部 |
分析 ①电离是电解质在水溶液中离解出自由移动离子的过程;
②电镀池实质是一个电解池;
③电解池是外加电源强迫下的氧化还原反应;
④电化学腐蚀原理是原电池原理.
解答 解:①电离是电解质在水溶液中离解出自由移动离子的过程,不需要通电,故①错误;
②电镀池实质是一个电解池,必须加外加电源故②正确;
③,电解池是外加电源强迫下的氧化还原反应,必须加外加电源,故③正确;
④电化学腐蚀原理是原电池原理,原电池中不含电源,是自发进行的氧化还原反应,故④错误.
故选B.
点评 本题是对电化学的电解池、原电池的构成条件的考查,要注意过程的发生需要的条件,难度不大.

练习册系列答案
相关题目
13. 某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
 某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )
某实验兴趣小组设计如下微型实验装置,a、b为直流电源的两极.实验时,若断开K1,闭合K2,两极均有气泡产生,下列有关描述正确的是( )| A. | 断开K1闭合K2时,总反应的离子方程式为:2H++2Cl-$\stackrel{电解}{→}$ H2↑+Cl2↑ | |
| B. | 断开K1闭合K2时,电子沿“a→Fe→电解质溶液→C→b”的路径流动 | |
| C. | 断开K1闭合K2时,铁电极附近溶液pH逐渐升高 | |
| D. | 断开K2闭合K1时,Fe电极被保护,此法称为牺牲阳极的阴极保护法 |
17.向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| A. | 先滴加BaCl2溶液再滴加HCl溶液,生成白色沉淀,原溶液中有SO42- | |
| B. | 滴加氯水和CCl4,振荡、静置,上层溶液显紫色,原溶液中有I- | |
| C. | 用洁净铁丝蘸取溶液进行焰色反应,火焰呈黄色,原溶液中有Na+ | |
| D. | 滴加NaOH溶液,将湿润红色石蕊试纸置于试管口,试纸不变蓝,原溶液中无NH4+ |
7.关于物质的量浓度溶液的配置说法正确的是( )
| A. | 容量瓶在使用之前要检漏 | |
| B. | 容量瓶上有温度,浓度,标线三个标识 | |
| C. | 定容时,因不慎使液面高于容量瓶的刻度线,可用滴管将多余液体吸出 | |
| D. | 配置好的溶液储存在容量瓶中,并贴上标签 |
12.NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,22.4L CHCl3含氯原子数为3NA | |
| B. | 100mL 1 mol•L-1醋酸溶液中的氢原子数为0.4NA | |
| C. | 常温常压下,11.2g乙烯中共用电子对数为2.4NA | |
| D. | 6.4 g CaC2晶体中所含的离子总数为0.3NA |
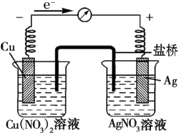 某探究小组将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag (s)设计成原电池,某时刻的电子流向及电流表(A)指针偏转方向如图所示.
某探究小组将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag (s)设计成原电池,某时刻的电子流向及电流表(A)指针偏转方向如图所示.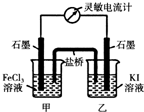 常温下,将FeCl3溶液和KI溶液混合,发生如下反应:2Fe3++2I-?2Fe2++I2
常温下,将FeCl3溶液和KI溶液混合,发生如下反应:2Fe3++2I-?2Fe2++I2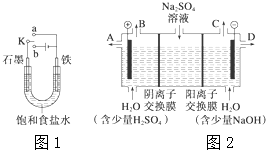 (1)某课外活动小组同学用图1装置进行实验,试回答下列问题:
(1)某课外活动小组同学用图1装置进行实验,试回答下列问题: