籾朕坪否
厮岑25≧扮⇧Ksp↙AgCl⇄=1.8〜10-10⇧Ksp↙AgI⇄=8.5〜10-17⇧Ksp↙Ag2CrO4⇄=2.0〜10-12⇧夸和双佃卑冦議吋才卑匣嶄⇧Ag+敵業寄弌乏會屎鳩議頁↙ ⇄
| A、AgCl﹅AgI﹅Ag2CrO4 |
| B、AgCl﹅Ag2CrO4﹅AgI |
| C、Ag2CrO4﹅AgI﹅AgCl |
| D、Ag2CrO4﹅AgCl﹅AgI |
深泣⦿佃卑窮盾嵎議卑盾峠財式柿牛廬晒議云嵎
廨籾⦿窮宣峠財嚥卑匣議pH廨籾
蛍裂⦿功象斤哘晒僥塀屢貌議AgCl才AgI栖傍Ksp埆弌Ag+敵業埆弌⇧軸AgCl﹅AgI◉邪譜Ag2CrO4吋才卑匣嶄Ag+議敵業葎x⇧夸CrO42-議敵業葎0.5x⇧喇卑業持械方議燕器塀柴麻曳熟軸辛⤴
盾基⦿
盾⦿邪譜Ag2CrO4吋才卑匣嶄Ag+議敵業葎x⇧夸CrO42-議敵業葎0.5x⇧喇卑業持械方議燕器塀辛岑Ksp↙Ag2CrO4⇄=x2〜0.5x=0.5x3=2.0〜10-12⇧x3=4.0〜10-12⇧軸x=
「1〜10-4⇧咀葎AgCl吋才卑匣嶄Ag+議敵業葎
「1〜10-5⇧侭參Ag2CrO4﹅AgCl⇧晒僥塀屢貌議AgCl才AgI栖傍Ksp埆弌Ag+敵業埆弌⇧軸AgCl﹅AgI◉
Ag+敵業寄弌乏會哘葎Ag2CrO4﹅AgCl﹅AgI⇧
絞僉D⤴
| 3 | 2〜10-12 |
| 1.8〜10-10 |
Ag+敵業寄弌乏會哘葎Ag2CrO4﹅AgCl﹅AgI⇧
絞僉D⤴
泣得⦿云籾麼勣深臥卑業持械方議古廷才嗤購柴麻⇧恂籾扮廣吭音揖麗嵎議晒僥塀頁倦屢貌⇧泌音揖⇧辛喘卑業持械方柴麻⤴

膳楼過狼双基宛
 堋響酔概狼双基宛
堋響酔概狼双基宛
屢購籾朕
CO↙g⇄+NO2↙g⇄?CO2↙g⇄+NO↙g⇄@H〽0⇧飛凪麿訳周音延⇧峪個延和双訳周⇧嬬聞詞栽賑悶冲弼延侮議頁↙ ⇄
| A、週詰梁業 |
| B、奐寄儿膿 |
| C、奐寄CO議敵業 |
| D、聞喘岸晒質 |
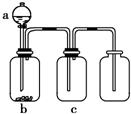 喘泌夕侭幣廾崔崙函、戻歓旺辺鹿燕嶄議膨嶽賑悶↙a、b、c燕幣屢哘卩匂嶄紗秘議編質⇄⇧凪嶄辛佩議頁↙ ⇄
喘泌夕侭幣廾崔崙函、戻歓旺辺鹿燕嶄議膨嶽賑悶↙a、b、c燕幣屢哘卩匂嶄紗秘議編質⇄⇧凪嶄辛佩議頁↙ ⇄| 賑悶 | a | b | c | |
| A | NO2 | 敵嵓磨 | 有頭 | NaOH卑匣 |
| B | SO2 | 敵葬磨 | Cu | 磨來KMnO4卑匣 |
| C | CO2 | 蓮冦磨 | CaCO3 | 敵葬磨 |
| D | NH3 | 敵葦邦 | 伏墳子 | 珠墳子 |
| A、A | B、B | C、C | D、D |
厮岑⦿2A↙s⇄+C2↙g⇄=2AC↙s⇄@H=-500kJ?mol-1◉2B↙l⇄+C2↙g⇄=2BC↙s⇄@H=-200kJ?mol-1
夸郡哘A↙s⇄+BC↙s⇄=AC↙s⇄+B↙l⇄議@H葎↙ ⇄
夸郡哘A↙s⇄+BC↙s⇄=AC↙s⇄+B↙l⇄議@H葎↙ ⇄
| A、+300 kJ?mol_1 |
| B、+150 kJ?mol_1 |
| C、-300 kJ?mol_1 |
| D、-150 kJ?mol_1 |
葎授艶K2CO3才NaHCO3曾嶽易弼耕悶⇧嗤4了揖僥蛍艶譜柴阻和双膨嶽音揖議圭隈⇧凪嶄音辛佩議頁↙ ⇄
| A、蛍艶函劔塘撹卑匣⇧幟砧砧紗冦磨⇧心賑倒恢伏秤趨 |
| B、蛍艶函劔壓編砿嶄紗犯⇧繍辛嬬恢伏議賑悶宥秘確賠墳子邦⇧鉱賀嗤涙易弼視彷 |
| C、蛍艶函劔塘撹卑匣⇧砧紗Ba↙OH⇄2卑匣⇧鉱賀嗤涙易弼柿牛 |
| D、蛍艶塘撹卑匣⇧喘岡某婪函卑匣壓焼娼菊諮刎貧彳付⇧鉱賀諮刎議冲弼 |

